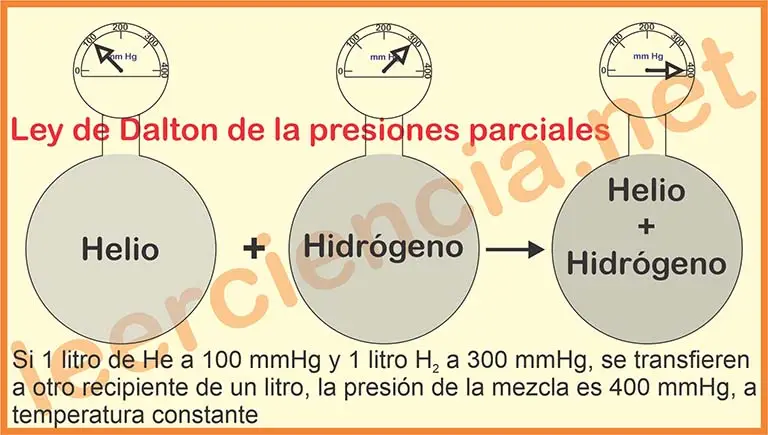
La ley de Dalton de las presiones parciales dice que, “En una mezcla de gases que no reaccionan químicamente, la presión total es la suma de las presiones parciales que cada uno de los gases ejercería si los otros no estuvieran presentes”. En otras palabras, la presión parcial de cada componente, es independiente de las presiones parciales de lo demás componentes. La fórmula de la ley de Dalton de las presiones parciales es:
P(total) = P1 + P2 + P3 + …
Donde P(total), es la presión ejercida por la mezcla y P es la presión parcial de cada componente.
¿Cómo se calcula la presión total?
La presión total se halla aplicando la ecuación de estado. Esta es:
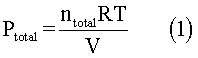
Donde n(total), es el número total de moles de los gases presentes en la mezcla. Además, R es la constante de los gases y T es la temperatura en grados Kelvin. Del mismo modo, V es el volumen medido en litros.
Ejemplo 1.
Se coloca 1 gramo de cada uno de los siguientes gases: H2, O2 y N2, en un recipiente de 8 litros a 12°C. Calcule la presión total en atmósferas.
Solución:
Primero, se calcula el número de moles de cada uno de los gases. esto se hace dividiendo la masa en gramos entre el peso molecular. Por lo tanto,
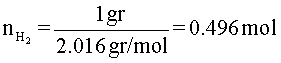
2.016 resulta de multiplicar el peso atómico del hidrógeno por 2. El peso atómico lo encuentra en la tabla periódica. Lo mismo ocurre con los otros 2 gases.
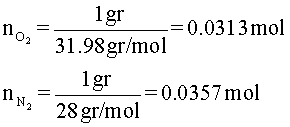
En consecuencia, el número total de moles es:
0.496 + 0.0313 + 0.0357 = 0.563 mol
Para terminar, se aplica la fórmula 1, teniendo en cuenta que 12°C equivalen a 285°K y que R tiene un valor de 0.082.
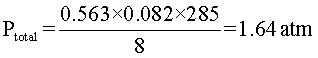
En resumen, la presión total de los 3 gases es de 1.64 atmósferas.
¿Cómo se halla la presión parcial de un gas en una mezcla?
La presión ejercida por un gas es proporcional al número de moléculas presentes del gas e independiente de su naturaleza. En general, la presión parcial de cualquier componente, en una mezcla de gases, se calcula multiplicando la presión total, por la fracción de la cantidad de moles de ese componente. Esta relación se expresa mediante la ecuación:
PA = XA × P(total) (2)
Donde A, representa un componente de la mezcla y X es la fracción de la cantidad de moles. XA se calcula con la siguiente fórmula:
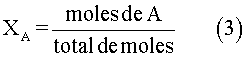
Ejemplo 2:
Se tiene una mezcla de gases formada por 78 gr de nitrógeno N2, 21 gr de oxígeno O2 y 1 gr de gas carbónico CO2. Si la presión de la mezcla es de 0.997 atmósferas ¿Cuál es la presión parcial del O2?
Solución:
Como en el ejemplo1, primero se halla el número de moles de cada gas, dividiendo la cantidad en gramos entre el peso molecular.
Entonces,
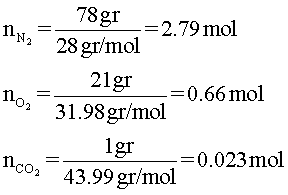
Para continuar, se calcula la fracción de la cantidad de moles de O2. Es decir, XO2 (Ecuación 3).
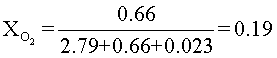
Para terminar, se halla la presión parcial del oxígeno O2, multiplicando XO2 por la presión total (ecuación 2).
PO2 = 0.19 × 0.997 atm = 0.189 atm.
En conclusión, la presión parcial de O2 en la mezcla dada, es de 0.189 atmósferas.
Aplicaciones de la ley de Dalton de las presiones parciales
La ley de Dalton de las presiones parciales tiene múltiples aplicaciones:
- Permite explicar por qué un atleta tiene más dificultad respiratoria para al competir a gran altitud. Con el aumento de la altitud, disminuye la presión atmosférica, es decir, la presión total del aire. En consecuencia, disminuye la presión parcial del oxígeno, haciendo más difícil su asimilación.
- Sirve para diseñar sistemas de almacenamiento de gases.
- Se usa en la producción de gases industriales.
- Se usa, obviamente, para calcular la presión total de una mezcla de gases y la presión parcial de un gas en una mezcla.
Taller de lectura
- Escriba el enunciado de la ley de Dalton de las presiones parciales.
- ¿Cómo se halla la presión total de una mezcla de gases?
- Escriba la ecuación (1).
- Copie el ejemplo 1, con el procedimiento.
- ¿Cómo se calcula la presión parcial de un gas en una mezcla?
- Copie la ecuación (2).
- Escriba la ecuación (3) y, además, escriba para qué se usa.
- Copie el ejemplo 2, con el procedimiento.
- ¿Para que se usa la ley de Dalton de las presiones parciales?
