Los gases ideales son aquellos cuyo comportamiento encaja en las leyes estudiadas por los científicos. Por ejemplo, en la ley de Boyle, en la ley de Charles y en el principio de Avogadro. Es decir que, su comportamiento permite comparar y medir todas sus propiedades.
Propiedades de los gases ideales
Las propiedades de los gases ideales se resumen en tres enunciados:
- A temperatura constante, el volumen de un gas es inversamente proporcional a la presión.
- Manteniendo la presión constante, el volumen de un gas es directamente proporcional a la presión.
- A temperatura y presión constantes, el volumen de un gas es directamente proporcional a su cantidad expresada en moles (n).
Estas propiedades se cumplen, particularmente, a altas temperaturas y presiones bajas. Además, su combinación permite enunciar la ley de los gases ideales.
Ley de los gases ideales
Esta ley establece que la presión (P), el volumen (V) Y la temperatura (T) de una cantidad de gas dada en moles (n), se relacionan mediante la expresión:
PV = nRT
Esta relación se conoce como la ecuación de estado de un gas ideal. Una ecuación de estado es la que relaciona variables que pueden usarse para definir o describir el estado de un sistema.
Además, las unidades a utilizar en esta ecuación son: grados Kelvin para la temperatura, litros para el volumen, atmósferas para la presión y moles para la cantidad de gas.
Para poder utilizar la ecuación de estado, es necesario conocer el valor numérico de la constante universal de los gases, que se representa con R.

Constante universal de los gases
El cálculo de esta constante, se obtiene a partir de condiciones de presión, temperatura y volumen molar de un gas, que se denominan condiciones estándar o TPS y son las siguientes:
- Presión = 1 atmósfera.
- Temperatura = 273,15°K.
- Volumen molar = 22.414 litros.
Despejando R, de la ecuación de estado, reemplazando valores y operando, tenemos:
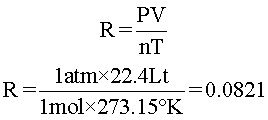
En conclusión, la constante universal de los gases es 0,0821 y sus unidades son litro por atmósfera, sobre grados Kelvin por mol.
Ejercicios resueltos de gases ideales
Cálculo del volumen
¿Qué volumen ocupan 10 gramos de nitrógeno N2, a una presión de 0,3 atmósferas y 400°K de temperatura?
Datos del ejercicio
- P = 0,3 atm.
- T = 400°K.
- Cantidad de gas N2, 10gr.
Procedimiento
La presión y la temperatura están en las unidades adecuadas, pero la cantidad de gas debe expresarse en moles. Por lo tanto, primero debe hacerse la conversión.
Se sabe que la masa atómica del nitrógeno es 14gr y, en consecuencia, la masa molecular del N2, es 28gr. Entonces:
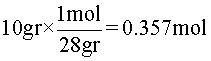
Como resultado, 10 gramos de N2, equivalen a 0,357 moles.
Después de eso, se puede utilizar la ecuación de estado para despejar volumen, reemplazar valores y realizar las operaciones.
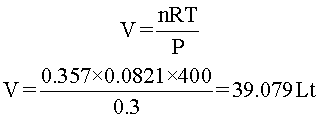
Respuesta: los 10 gramos de nitrógeno N2, ocupan un volumen de 39,079 litros
Cálculo de la presión
¿Qué presión soportan 2,5×1020 moléculas de CO2, en un recipiente de 750ml a 325°K?
Datos del ejercicio
- T = 325°K.
- V = 750ml.
- cantidad de gas: 2,5×1020 moléculas de CO2.
Procedimiento
En este caso es necesario representar el volumen en litros y la cantidad de gas en moles.
Conversión del volumen:
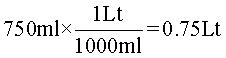
Conversión de la cantidad de gas en moles. Para esto, se multiplica la cantidad de moléculas (2,5×1020), por el factor de conversión que indica que, un mol equivale a 6,02×1023 moléculas.
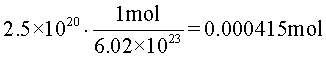
Para terminar, se utiliza la ecuación de estado para despejar presión, reemplazar valores y realizar las operaciones.
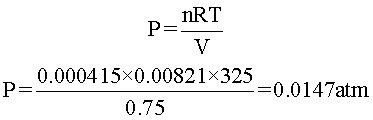
Respuesta: La presión que soportan las 2,5×1020 moléculas de CO2 es 0,0147 atmósferas.
Cálculo de la temperatura
¿A qué temperatura se encuentran 0,95 moles de O2, en un recipiente de 0,5litros, si la presión 1,2 atmósferas?
Datos del ejercicio
- cantidad de gas = 0,95 moles.
- V = 0,5 litros.
- P = 1,2 atmósferas.
Procedimiento
En este caso todos los datos están en las unidades adecuadas y, por lo tanto, se puede utilizar la ecuación de estado, despejar temperatura, reemplazar valores y realizar las operaciones directamente.
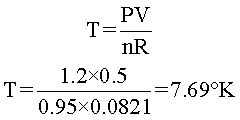
Respuesta: los 0,95 moles de O2, se encuentran a una temperatura de 7,69 grados Kelvin.
Cálculo del número de moles
¿Cuántas moles de cloro Cl2, hay en un recipiente de 0,25 litros, sometidas a una presión de 3,4 atmósferas y 60°C de temperatura?
Datos del ejercicio
- V = 0,25 litros.
- P = 3,4 atmósferas.
- T = 60 grados centígrados.
Procedimiento
Volumen y presión están en las unidades adecuadas, pero la temperatura debe representarse en grados Kelvin.
Conversión de la temperatura:
°K = °C + 273
°K = 60 + 273 = 333
A continuación, se puede utilizar la ecuación de estado, despejar número de moles, reemplazar valores y realizar las operaciones.
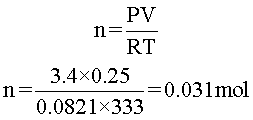
Respuesta: en el recipiente hay 0,031 moles de Cl2.
Taller de lectura
- ¿Qué son gases ideales?
- Escriba las propiedades o características de los gases ideales.
- Copie la ecuación de estado delos gases ideales y, además escriba qué es una ecuación de estado.
- ¿En qué unidades deben estar la temperatura, el volumen, la presión y la cantidad de gas, para usarlas en la ecuación de estado?
- Escriba el valor de la constante universal de los gases.
- Copie, con el procedimiento respectivo, los 4 ejercicios resueltos.
