La ley combinada de los gases establece la forma como cambia el volumen o la presión o la temperatura, si se conocen las condiciones iniciales y dos de las condiciones finales. Las condiciones iniciales se representan con (Pi, Vi, Ti). Por otro lado, las condiciones finales son (Pf, Vf, Tf). Esta ley resulta de la combinación de otras leyes de los gases, como las leyes de Charles y de Boyle.
Esta ley se usa para calcular el tamaño de un tanque que debe almacenar cierta cantidad de gas, a temperatura y presión determinadas. También, sirve para analizar como la temperatura y la presión atmosférica influyen en la formación de nubes. En general, sirve para extrapolar el comportamiento de los gases al variar sus condiciones de volumen, presión o temperatura.
Fórmula de la ley combinada de los gases
Esta fórmula relaciona las condiciones iniciales de un gas con sus condiciones finales. Dicha relación es escribe como:
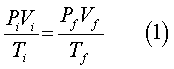
La razón PV/T es constante.
De esta ecuación se pueden obtener fórmulas para Pf, Vf y Tf.
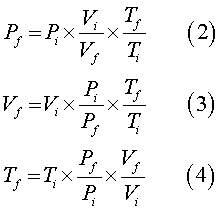
Ejemplos de la ley combinada de los gases
Ejemplo 1
2.65 litros de un gas a 25°C y 1 atm de presión, se calienta y se comprime 75°C y 2 atm. ¿Cuál es su volumen final?
Solución:
Para empezar, se organizan los datos en una tabla como la siguiente:
| P (atm) | T (°K) | V (Lt) | |
|---|---|---|---|
| Inicial | 1 | 25+273=298 | 2.65 |
| Final | 2 | 75+273=348 | ? |
Como se debe calcular el volumen final Vf, se aplica la fórmula (3), Se reemplazan los valores y se hacen las operaciones.
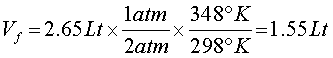
En resumen, el volumen final del gas es de 1.55 litros.
Ejemplo 2
Un tanque contiene 6m3 de helio a 10°C y una atmósfera de presión. Si se traslada todo el gas a otro tanque de 1.5m3 y se almacena a 20°C ¿Cuál es la presión del gas en el segundo recipiente?
Solución:
Inicialmente, se organizan los datos
| P (atm) | T (°K) | V (Lt) | |
|---|---|---|---|
| Inicial | 1 | 10+273=283 | 6000 |
| Final | ? | 20+273=293 | 1500 |
Nota: 6m3 equivalen a 6000 litros porque cada metro cúbico equivale a 1000 litros. Por lo mismo, 1.5 m3, equivalen a 1500 litros.
Después de eso, se aplica la ecuación (2) para hallar la presión final.
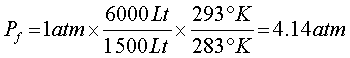
En conclusión, la presión final del gas es de 4.14 atmósferas.
Taller de lectura
- ¿Qué establece la ley combinada de los gases?
- ¿Cómo se representan las condiciones iniciales y las condiciones finales?
- ¿Cuáles son los usos de la ley combinada de los gases?
- Copie la fórmula (1) y las fórmulas para calcular Pf, Vf y Tf.
- Escriba los ejercicios resueltos con el procedimiento.

