Los alquenos, son aquellos hidrocarburos que tienen, por lo menos, un enlace doble entre átomos de carbono. Se clasifican, junto con los alquinos, dentro de los hidrocarburos insaturados, por su capacidad para reaccionar con hidrógeno. El más simple de ellos, es el eteno o etileno CH2=CH2. En esta molécula, todos los núcleos de los átomos de carbono e hidrógeno están en el mismo plano. Además, tienen ángulos de enlace de 120°.
Estructura de los alquenos
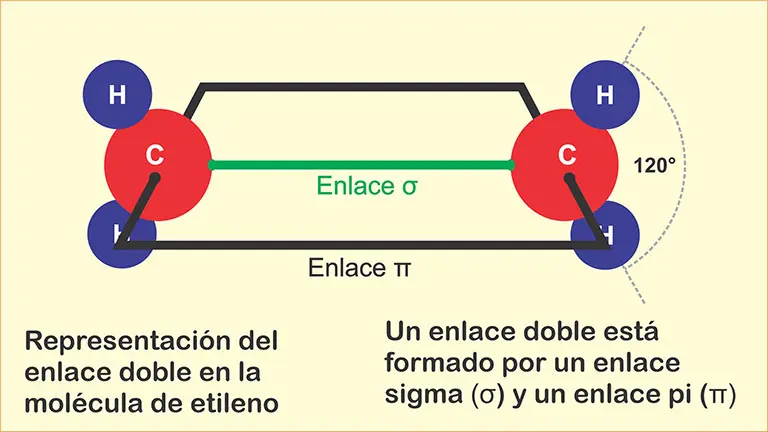
Los carbonos que forman el enlace doble, tienen hibridación sp2. Por lo tanto, comparten 2 electrones en un enlace sigma (σ) y 2 en un enlace pi (π). El enlace σ, se ubica en la línea que une los carbonos. Por su parte, el enlace π forma una nube electrónica por delante y por detrás del primero (figura 1). Además, el enlace π es importante en el comportamiento químico de los alquenos por ser más reactivo. Por esta razón, al doble enlace carbono – carbono, se le considera como el grupo funcional de los alquenos. La fórmula general de los alquenos que tienen solo un enlace doble es CnH2n.
Obtención o preparación de los alquenos
A nivel industrial, los alquenos se obtienen del petróleo y por destilación de la huya. Sin embargo, a nivel de laboratorio, se pueden obtener a través de dos reacciones: deshidrohalogenación de halogenuros de alquilo y por deshidratación de alcoholes.
1 – Deshidrohalogenación de halogenuros de alquilo
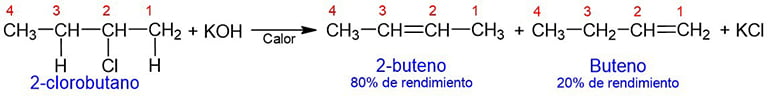
El halogenuro de alquilo se hace reaccionar con hidróxido de potasio concentrado en etanol y a alta temperatura. En la reacción se elimina un mol de haluro de hidrógeno y se forma el alqueno correspondiente. En la reacción se pueden formar dos alquenos, pero se obtiene en mayor proporción el más estable, según la regla de Saytzeff. Esta regla dice que el alqueno más estable es el que presenta mayor sustitución del doble enlace por grupos alquilo. En otras palabras, el alqueno más estable es aquel donde, el enlace doble, se forma entre átomos de carbono con el menor número de hidrógenos.
2 – Deshidratación de alcoholes
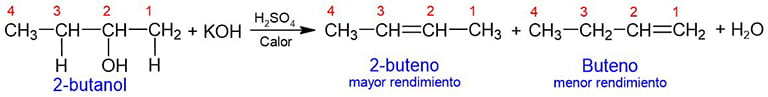
Consiste en la eliminación de una molécula de agua de un alcohol. La reacción se lleva a cabo calentando el alcohol en medio ácido. También, pasando el vapor del alcohol sobre polvo de óxido de aluminio (Al2O3) a 300°C. Esta es otra reacción que sigue la regla de Saytzeff.
Propiedades físicas de alquenos
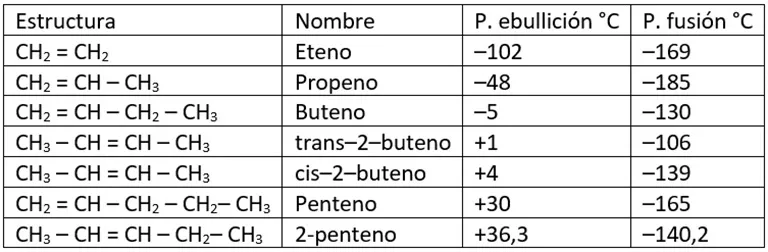
Las propiedades físicas de alquenos son muy parecidas a las de los correspondientes alcanos. Es decir, los primeros 3 de la serie (eteno, propeno y buteno), son gases; del C5 al C18 son líquidos y los superiores son sólidos. Son apolares, insolubles en agua, pero se disuelven en solventes orgánicos. A diferencia de los alcanos, se disuelven en ácido sulfúrico concentrado y frío. Por lo tanto, esta propiedad es útil para separarlos de los alcanos. Adicionalmente, los puntos de ebullición aumentan al aumentar el peso molecular (tabla 1) y sus densidades oscilan entre 0,6gr/ml y 0,7gr/ml.
Propiedades químicas de los alquenos
Los alquenos reaccionan fácilmente con una variedad de reactivos. Los principales tipos de reacciones en las que participan son: adición, reducción, oxidación y polimerización.
Reacciones de adición
En este tipo de reacción, dos átomos o grupos de átomos, se unen a los carbonos que forman el enlace doble. Entre los reactivos que se adicionan están, por ejemplo, los haluros de hidrógeno, los halógenos, el ácido sulfúrico y el agua. Normalmente, las reacciones de adición cumplen la regla de Markovnikov. Según esta regla, “el hidrógeno del reactivo que se adiciona, se une al carbono del enlace doble, que tenga el mayor número de hidrógenos unidos a él”. Es importante tener en cuenta, que la regla no se cumple al 100% y que es posible obtener dos isómeros en la reacción. No obstante, el isómero que sigue la regla, se produce en mayor cantidad y se llama “producto principal”.
1 – Hidrohalogenación
Es la adición de un haluro de hidrógeno (HCl, HBr o HI) a un alqueno, para producir haluro de alquilo. Por ejemplo, la adición de HCl al buteno es:
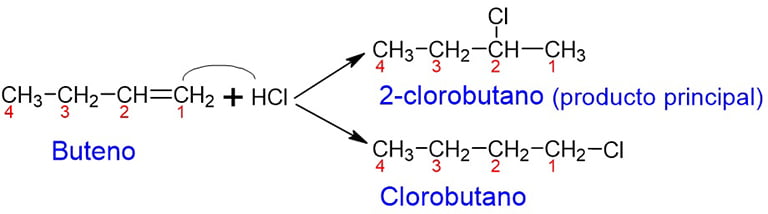
En el ejemplo anterior, el 2-clorobutano (producto principal) cumple la regla de Markovnikov. Es decir, el hidrógeno del HCl, se une al carbono 1 que tiene 2 hidrógenos y el cloro, va al carbono 2. En el clorobutano, acurre lo contrario.
2 – Halogenación
Es la adición de un halógeno como Cl2 o Br2. La reacción ocurre bajo condiciones normales de temperatura y presión, pero en presencia de tetracloruro de carbono (CCl4) como catalizador. Por ejemplo,
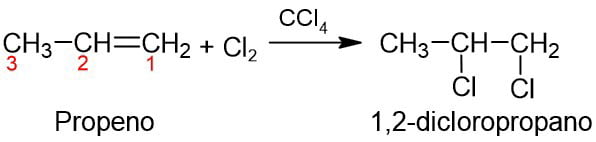
3 – Adición de ácido sulfúrico
La reacción da como resultado un bisulfato que, si se disuelve en agua y se calienta, produce un alcohol. Esta reacción es, además, uno de los mejores métodos para sintetizar alcohol en el laboratorio.
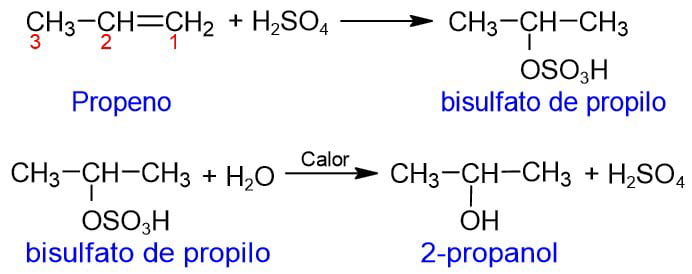
4 – Reacción de hidratación
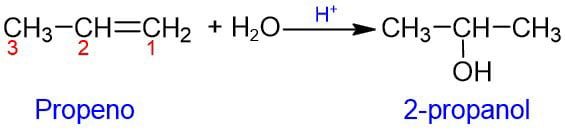
Consiste en la reacción de un alqueno con el agua. La reacción se desarrolla en medio ácido y da como producto un alcohol. Primero, la molécula de agua se disocia formando un ion H+ y uno OH–. Después, el H+ va a un carbono del enlace doble y el OH– al otro, siguiendo la regla de Markovnikov.
Reacciones de reducción
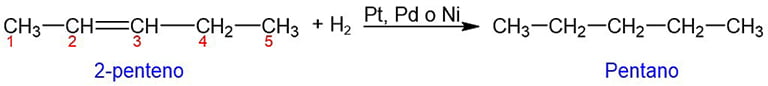
Los alquenos reaccionan con hidrógeno en presencia de Pt, Pd o Ni como catalizador. El resultado es, Por lo tanto, un alcano. Por ejemplo, de la hidrogenación del 2-penteno se obtiene pentano.
Reacciones de oxidación
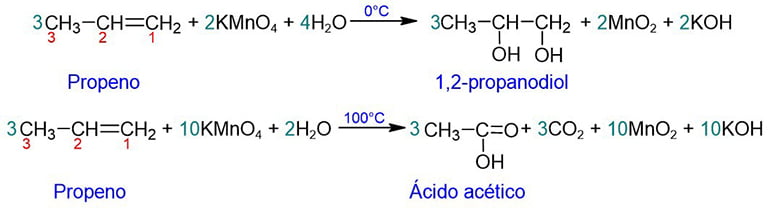
Los alquenos se oxidan (parcialmente) al reaccionar con permanganato de potasio y agua. En frío, se obtiene un dialcohol. Esta reacción es útil para reconocer los alquenos (prueba de Bayer). A 100°C, sin embargo, esta reacción puede producir ácidos carboxílicos, cetonas o CO2.
Reacciones de polimerización
Las reacciones de polimerización de los alquenos, son las más importantes desde el punto de vista industrial. De ellas se obtienen, por ejemplo, polietileno, polipropileno, polibutadieno y poliestireno. Además, estas reacciones están estrechamente relacionadas con la producción de otros polímeros como el cloruro de polivinilo (PVC) y el acetato de polivinilo (PVA).
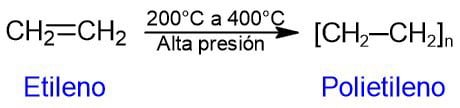
Cuando se calienta etileno (o eteno) a temperaturas entre 200°C y 400°C y se somete a altas presiones, se obtiene polietileno. El polietileno es un polímero saturado de cadena muy larga y peso molecular muy elevado. El polietileno se usa para fabricar, por ejemplo, bolsas, envases, cintas adhesivas, juguetes, elementos de cocina, aislantes eléctricos, bolígrafos desechables y cientos de productos más.
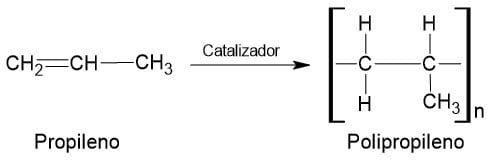
El polipropileno es un polímero termoplástico que resulta de la polimerización del propileno (o propeno) CH2=CH─CH3. Se emplea en multitud de artículos como cajas y contenedores para el transporte, envase alimentario, menaje doméstico, muebles y armarios. Presenta buen balance entre rigidez e impacto, protección UV, antiestático y antideslizante.
El polibutadieno o caucho sintético se obtiene por polimerización del 1,3 butadieno CH2=CH─CH=CH2. Aunque se utiliza en infinidad de productos, el 70% de la producción mundial se destina a la fabricación de neumáticos para auto.
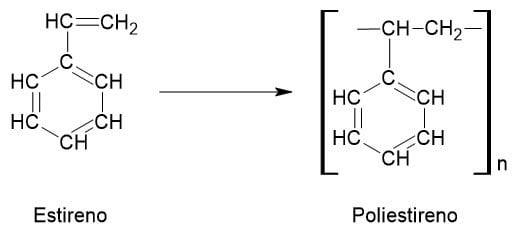
El poliestireno resulta de la polimerización del estireno o etenilbenceno. El más conocido es el poliestireno expandido que, además, tiene múltiples nombres comunes, por ejemplo, unicel, icopor, porexpan y Telgopor entre otros. Sin embargo, hay otras 3 clases de poliestireno que se usan en la fabricación de platos, vasos, cubiertos y otros recipientes desechables. También, en construcción como aislante térmico y acústico.
Nomenclatura de los alquenos
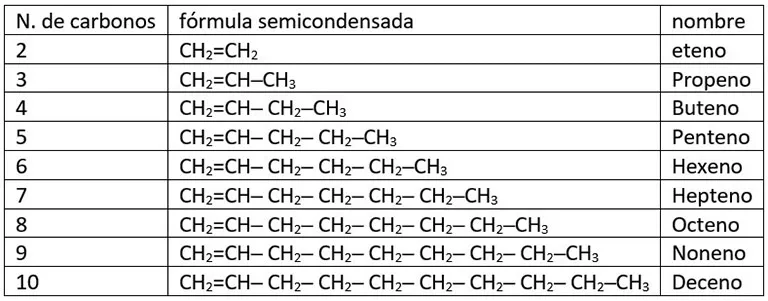
A – Los alquenos con cadena abierta no ramificada y un único enlace doble entre los carbonos 1 y 2, se nombran usando un prefijo y un sufijo. Un prefijo que indica el número de carbonos y, además, el sufijo “eno” que identifica a los alquenos. La tabla 2 muestra los nombres de los primeros 9.
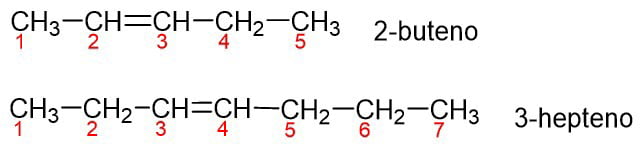
B – Si el enlace doble no está en el primer carbono, se usa el número del carbono donde está el enlace doble para ubicarlo. Primero, se enumera la cadena de carbono iniciando por el extremo más cercano al doble enlace. Por ejemplo,
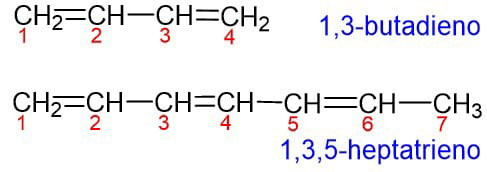
C – Si el alqueno tiene más de un enlace doble, se usan prefijos di, tri, etc., antes de la terminación eno.
D – Si el compuesto tiene grupos alquilo unidos a la cadena principal, se ubican asignando el número de carbono al que están unidos. Después de eso se nombra el enlace doble.
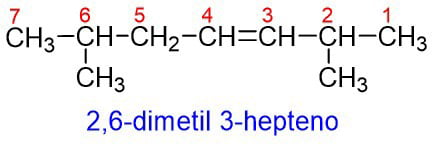
E – Si la cadena es más compleja, se selecciona como cadena principal, aquella que tenga la mayor cantidad de enlaces dobles.
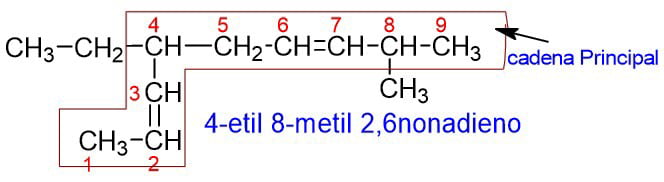
F – En los cicloalquenos se antepone la palabra ciclo al nombre de la cadena principal.
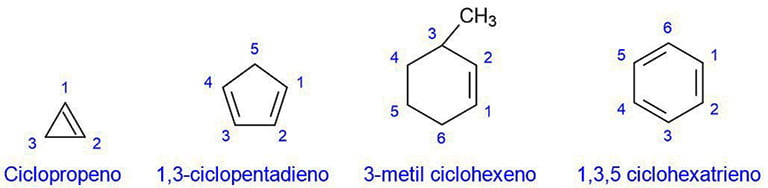
Usos y aplicaciones de los alquenos
De los alquenos se obtienen fácilmente otros grupos funcionales, que son intermedios importantes en la síntesis de cientos de sustancias de importancia industrial. Del etileno (eteno), por ejemplo, se obtiene polietileno, alcohol etílico, etilenglicol, cloruro de vinilo, etenilbenceno, acetato de etilo y cerca de 50 productos más. El propeno, por su parte, se utiliza en la producción de polipropileno y alcohol isopropílico. Igualmente, el 1,3-butadieno se usa en la producción de caucho y en la síntesis de algunos alcoholes y cetonas. El isobutileno (2-metilpropeno), usa en la preparación del isooctano (2,2,4-trimetilpentano), combustible de grado 100 en la asignación de octanaje de la gasolina.
Taller de lectura
- ¿Qué son los alquenos y por qué se clasifican dentro de los hidrocarburos insaturados?
- ¿Cómo se ubican los enlaces σ y los enlaces π, en el enlace doble?
- ¿Cuál es el grupo funcional de los alquenos?
- Copie la figura 1.
- Haga un resumen de las propiedades físicas de los alquenos y, además, copie la tabla 1.
- ¿Cuáles son los tipos de reacción en las que participan los alquenos?
- ¿En qué consiste la regla de Markovnikov?
- Defina las 4 reacciones de adición y, además escriba un ejemplo de cada una.
- Escriba la definición de las reacciones de reducción y oxidación. Adicionalmente, escriba un ejemplo de cada una.
- ¿Por qué son importantes las reacciones de polimerización?
- Escriba la definición, obtención y usos del polietileno, polipropileno, polibutadieno y poliestireno.
- ¿Cuáles son los usos y aplicaciones de los alquenos?
- ¿En qué consiste la regla de Saytzeff?
- ¿Cuáles son los métodos de obtención de alquenos? Escriba los ejemplos.
- ¿Cómo se nombran los alquenos con cadena abierta no ramificada y un único enlace doble entre los carbonos 1 y 2? Además, escriba 3 ejemplos de la tabla 2.
- Haga un resumen de los literales B, C, D, E y F donde se explica la nomenclatura de los alquenos. Adicionalmente, copie un ejemplo de cada uno.
