El carbono es un elemento incluido en el grupo IVA y periodo 2 de la tabla periódica.
En la naturaleza, se encuentra como carbono puro o elemental, en dos formas alotrópicas. Grafito y diamante. Las formas alotrópicas de un elemento se diferencian por la forma de sus cristales. El diamante, por ejemplo, forma cristales cúbicos u octaédricos que son incoloros. Este elemento también existe como carbono amorfo. El carbono amorfo no forma cristales. Por ejemplo, la hulla y la antracita, son de este tipo. En resumen, hay dos clases de carbono: cristalino y amorfo.
El carbono también se encuentra formando compuestos inorgánicos como monóxido, dióxido, bisulfuro y tetracloruro de carbono. Del mismo modo, forma sales como los carbonatos y los carburos. Sin embargo, los compuestos del carbono que cobran mayor importancia hoy, son los compuestos orgánicos. Los compuestos orgánicos están relacionados con los seres vivos, los derivados del petróleo y los plásticos en general. Al estudio de los compuestos orgánicos se le llama química del carbono.
Propiedades del carbono
| Número atómico (Z) | 6 |
| Masa atómica (uma) | 12,01 |
| Electrones de valencia | 4 |
| Electronegatividad | 2,5 |
| 1ª energía de ionización (KJ/mol) | 1090 |
| Energía de enlace C-C (KJ/mol) | 356 |
| Energía de enlace C-H (KJ/mol) | 414 |
La electronegatividad del carbono no es tan débil como para ceder sus 4 electrones de valencia, ni tan fuerte como para obtener 4 electrones de otro elemento, durante una reacción. En otras palabras, no tiende a formar cationes C+4 ni aniones C-4. En consecuencia, este elemento forma, generalmente, enlaces covalentes. Es decir, comparte sus 4 electrones de valencia con otros átomos, para obtener una configuración estable. En resumen, el carbono es tetravalente y sus enlaces pueden distribuirse en 4 enlaces sencillos, o un enlace doble y dos sencillos, o dos enlaces dobles, o uno sencillo y uno triple.
Por otro lado, debido a la alta energía de enlace entre átomos de carbono, este elemento tiene una fuerte tendencia a formar cadenas y anillos, dando origen a una infinita variedad de moléculas. La propiedad de los átomos de carbono para unirse entre sí, se llama concatenación.
Configuración electrónica e hibridación
El número atómico indica que, en su estado basal, el carbono tiene 6 electrones. Dos en el primer nivel y 4 en el segundo nivel o capa de valencia. Entonces, la configuración electrónica del carbono es 1s2, 2s2, 2p2, o bien:
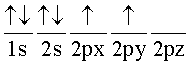
Observe que hay 2 electrones desapareados en dos orbitales 2p según la regla de Hund. por lo tanto, este átomo sólo formaría dos enlaces covalentes. Sin embargo, la evidencia obtenida por difracción de rayos x, muestra que esto no es así. El metano (CH4), por ejemplo, muestra 4 enlaces simétricos.
Si uno de los electrones del orbital 2s, se mueve al orbital vacío 2pz, se tendría la siguiente configuración:
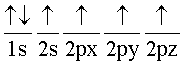
Esta configuración explica los 4 enlaces covalentes, pero no la simetría entre ellos, puesto que los orbitales 2s y 2p tienen valores energéticos diferentes. En consecuencia, se requiere que dichos orbitales se combinen tomando valores intermedios. La combinación de orbitales se denomina hibridación y a los orbitales resultantes, se les llama orbitales híbridos. Por otro lado, los orbitales híbridos se nombran de acuerdo con los orbitales que los forman. En este caso, por ejemplo, participa un orbital s y tres orbitales p (px, py pz). En consecuencia, el orbital híbrido se llama sp3. La tabla 2 muestra los tipos de orbitales híbridos y la geometría de los enlaces que forman.
| Orbitales hibridados | Nombre de la hibridación | Geometría | Ángulo de enlace (aproximado) |
|---|---|---|---|
| un s y un p | sp | lineal | 180° |
| un s y dos p | sp2 | Trigonal | 120° |
| un s y tres p | sp3 | tetraédrica | 109,5° |
Propiedades de los orbitales híbridos y puros
En general, los orbitales híbridos forman enlaces más fuertes y estables que los formados por orbitales puros. Su nube de electrones es simétrica alrededor del eje que une los núcleos de los átomos enlazados. Además, los enlaces que forman, reciben el nombre de enlaces sigma (σ).
Por otro lado, los orbitales puros (p) forman enlaces llamados pi (π), cuyas nubes de electrones se ubican por «enzima» y por «debajo» del del eje que une los núcleos de los átomos enlazados.
Enlaces sencillos, dobles y triples entre átomos de carbono
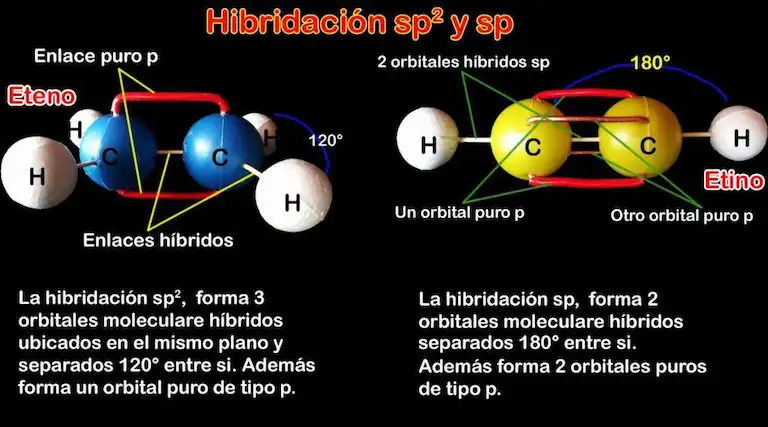
Primero, los enlaces sencillos, en compuestos saturados, están formados por enlaces sigma con hibridación sp3 (figura 1). Del mismo modo, los enlaces dobles están formados por un en lace sigma de hibridación sp2 (figura 2) y un enlace pi, constituido por un orbital p. Además, los enlaces triples se forman por un enlace sigma de hibridación sp, y dos enlaces pi, en los que participan dos orbitales p. Sin embargo, orbitales híbridos sp2 y sp (figura 2), también forman enlaces sencillos con carbonos adyacentes a un doble o triple enlace entre átomos de carbono.

Taller de lectura
- Escriba en qué se diferencian las formas alotrópicas de un elemento y, además, en qué formas alotrópicas se encuentra el carbono.
- Cite dos ejemplos de carbono amorfo.
- Escriba 3 ejemplos de compuestos inorgánicos y 3 orgánicos de carbono.
- copie la tabla 1.
- ¿Por qué el carbono forma enlaces covalentes?
- ¿A qué se le llama concatenación?
- Copie el esquema de la configuración electrónica del carbono.
- Escriba la definición de hibridación y, además, de orbitales híbridos.
- Copie la tabla 2.
- Escriba las propiedades de los orbitales híbridos y, también, de los orbitales puros.
- ¿Cómo se forman los enlaces sencillos, dobles y triples?
- Copie las figuras 1 y 2.
