Los alcanos son compuestos orgánicos formados por carbono e hidrógeno, que se caracterizan porque todos los enlaces entre átomos de carbono son sencillos. Por un lado, los compuestos formados, únicamente, por carbono e hidrógeno se llaman hidrocarburos. Por otro lado, si tienen solo enlaces sencillos entre átomos de carbono, se llaman hidrocarburos saturados. Es decir, los alcanos son hidrocarburos saturados.
Características de los alcanos
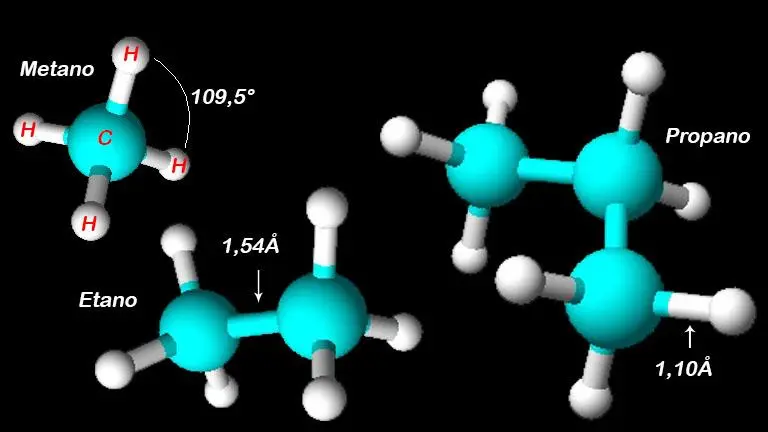
En los alcanos, cada átomo de carbono tiene 4 enlaces sencillos, formados por orbitales híbridos del tipo sp3. Dichos orbitales generan una estructura tetraédrica con ángulos de 109,5° entre los enlaces. Por otro lado, los enlaces carbono–carbono y carbono-hidrógeno son enlaces sigma (σ). Los enlaces sigma son aquellos que tienen una forma simétrica alrededor de la línea que une los núcleos de los dos elementos. En los alcanos, los enlaces C–H tienen una longitud de 1,10Å (Angstrom). Un Angstrom equivale a una diez-mil-millonésima parte de un metro (1Å = 10-10m). Los enlaces C–C, por su parte, tienen una longitud de 1,54Å. Ver figura 1.
Métodos de preparación de alcanos
A nivel industrial, los alcanos se obtienen por destilación del petróleo y de la hulla. Sin embargo, a nivel de laboratorio, se pueden obtener mediante varios procesos.
1 – Hidrogenación de alquenos
Consiste en la adición catalítica de hidrógeno a un alqueno. Durante la reacción, se rompen los enlaces dobles y se forman enlaces sencillos. El catalizador puede ser platino, paladio o níquel.
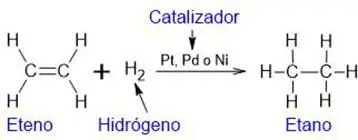
2 – Reducción de halogenuros de alquilo
Consiste en la sustitución de un átomo de halógeno por hidrógeno. Hay varias reacciones para lograr la reducción de un halogenuro de alquilo. Dos de ellas son, la reacción de Wurtz y la hidrólisis del reactivo de Grignard.
2.1 – Reacción de Wurtz
Consiste en hacer reaccionar dos halogenuros de alquilo para unirlos y formar un alcano de cadena más larga. El proceso se ilustra en el siguiente ejemplo.
2CH3–Cl + 2Na ⟶ CH3–CH3 + 2NaCl
Según la reacción anterior, 2 moles de cloro-metano reaccionan con 2 de sodio, para formar una mol de etano y 2 de cloruro de sodio.
2.2 – Hidrólisis del reactivo de Grignard
Este reactivo se prepara haciendo reaccionar un halogenuro de alquilo con magnesio en presencia de éter. Dicho reactivo, también se conoce con el nombre de haluro de alquilmagnesio. Además, su fórmula general es R-Mg-x (R representa una cadena de carbono y x representa un halógeno). En la siguiente reacción, el yodo-metano (CH3-I) (un halogenuro de alquilo) se combina con magnesio para formar yoduro de metil-magnesio (CH3-MgI) (reactivo de Grignard).

La reacción se desarrolla en dos pasos. Primero, se forma el reactivo de Grignard según la reacción anterior. Segundo, el reactivo de Grignard reacciona con agua para formar el alcano y otros compuestos. Por ejemplo, el yoduro de metil-magnesio (CH3-MgI) reacciona con agua para formar metano (CH4).
CH3–MgI + H2O ⟶ CH4 + MgOHI
Propiedades físicas de los alcanos
- Estado
- los cuatro primeros miembros de la serie son gases. Del pentano (C5H12) al hexadecano (C16H34) son líquidos. Por su parte, los alcanos con más de 16 átomos de carbono son sólidos y se les llama parafinas.
- Solubilidad
- Los alcanos son sustancias no polares. En consecuencia, debe disolverse en solventes orgánicos no polares. Son insolubles en agua, por lo cual se dice que son hidrofóbicos.
- Densidad
- Por lo general, los alcanos son menos densos que el agua. La densidad de estos compuestos es en promedio de 0,7 gr/ml. Al ser insolubles en agua, se separan fácilmente de ella formando una fase superior en la mezcla. Tal vez haya visto, por ejemplo, una mezcla de agua y gasolina en un recipiente de vidrio. La gasolina ocupa la parte superior de la mezcla.
- Punto de ebullición
- En los alcanos, el punto de ebullición aumenta gradualmente, al aumentar el número de átomos de carbono. En otras palabras, el punto de ebullición aumenta, al aumentar la masa molecular. Esto se debe a que las moléculas grandes tienen áreas superiores que generan fuerzas de atracción intermolecular (fuerzas de Van Der Waals) más grandes. Sin embargo, los alcanos ramificados tienen puntos de ebullición menores, que los no ramificados con el mismo número de carbonos.
- Puntos de fusión
- Esta propiedad también aumenta al aumentar la masa molecular. Los alcanos ramificados funden a mayor temperatura que los no ramificados con igual número de carbonos. La tabla 1 muestra la densidad, punto de ebullición y punto de fusión de algunos alcanos.
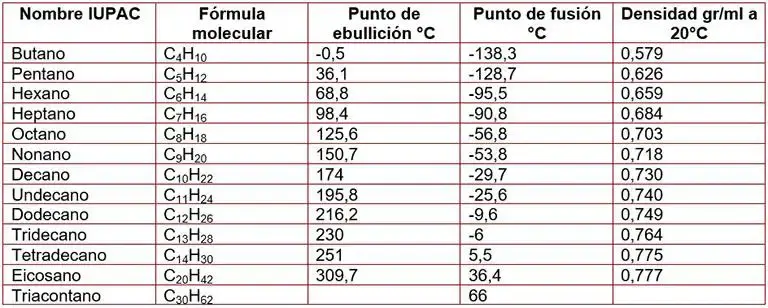
Propiedades químicas de los alcanos
Los alcanos son relativamente inertes en fase líquida. No obstante, en fase gaseosa y en presencia de catalizadores, pueden reaccionar de varias maneras. La reactividad de los alcanos de bajo peso molecular, es mayor que la de los alcanos de alto peso molecular. Además, los alcanos ramificados son más reactivos que sus isómeros sin ramificar. Las reacciones más importantes en las que participan los alcanos son:
Combustión
Es una reacción de oxidación, en la que el alcano reacciona con suficiente oxígeno, para producir gas carbónico, agua y gran cantidad de energía. Es, por lo tanto, una reacción exotérmica. Por ejemplo, la siguiente reacción muestra la combustión del propano.
C3H8 + 5O2 ⟶ 3CO2 + 4H2O
Existe también la oxidación parcial, que se da en condiciones limitadas de oxígeno. Durante este tipo de oxidación, se obtienen compuestos como monóxido de carbono, hidrógeno, aldehídos y alcoholes. Por ejemplo, de la oxidación parcial de metano se obtiene metanol (un alcohol).
2CH4 + O2 ⟶ 2CH3–OH
Pirólisis
Es la descomposición de un compuesto por calor. Al calentar un alcano, se puede obtener una mezcla de alcanos y alquenos de menor peso molecular. Además, se puede obtener hidrógeno. Por ejemplo, cuando se calienta propano a 600 °C, se forma propeno e hidrógeno o eteno y metano . A medida que aumenta el peso molecular del alcano, se forman mezclas aún más complejas.

Deshidrogenación
Consiste en retirar átomos de hidrógeno de un alcano. La reacción ocurre a altas temperaturas y con los catalizadores adecuados. Durante la reacción se rompen enlaces C–H. Como resultado, se obtienen alquenos, cicloalcanos y compuestos aromáticos. La deshidrogenación del propano, por ejemplo, produce propeno e hidrógeno.
CH3–CH2–CH3 ⟶ CH3–CH=CH2 + H2
Por su parte, la deshidrogenación del hexano produce ciclohexano y si la reacción continua, se obtiene benceno.
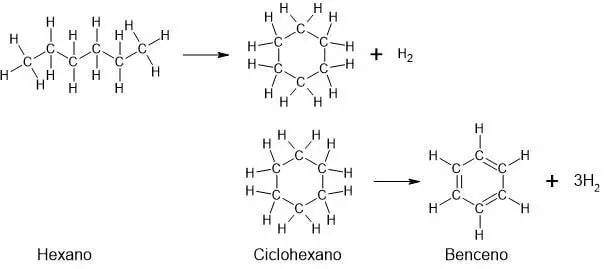
Isomerización
La isomerización consiste en la reacomodación de los átomos, para formar compuestos de igual peso molecular, pero diferente estructura. La reacción ocurre en presencia de ácido sulfúrico o tricloruro de aluminio como catalizador. El butano, por ejemplo, produce isobutano.
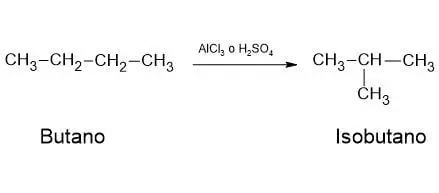
Alquilación
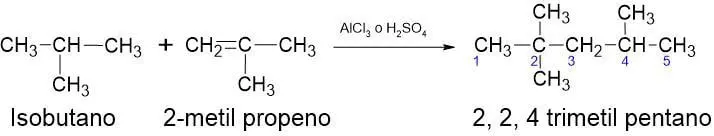
Consiste en la unión de un grupo alquilo con otra molécula. El proceso se puede ilustrar por la reacción de un alcano y un alqueno. La alquilación requiere ácido sulfúrico o tricloruro de aluminio como catalizador. Además, en esta reacción hay aumento de la ramificación y se obtienen productos de mayor peso molecular. Ver el siguiente ejemplo.
Halogenación
Es la adición de un halógeno a un alcano. La reacción requiere luz ultravioleta (LUV) como catalizador. Por ejemplo, al hacer reaccionar metano con Cl2, se obtiene cloro-metano.

Con suficiente cloro, la reacción puede continuar y producir diclorometano (CH2─Cl2), triclorometano o cloroformo (CH─Cl3) y tetraclorometano (CCl4).
Nitración
Consiste en la reacción de un alcano con ácido nítrico (HNO3). La reacción ocurre a altas temperaturas y da como producto, compuestos conocidos como nitroalcanos. Por ejemplo, si el etano reacciona con ácido nítrico, produce nitroetano.
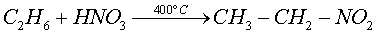
Clasificación de los alcanos
Los alcanos se dividen en dos grupos: los alcanos alifáticos y los cicloalcanos. Por un lado, los alcanos alifáticos se caracterizan por ser cadenas abiertas de átomos de carbono. La cadena puede ser “lineal” o ramificada. Si la cadena es “lineal” el alcano se denomina n-alcano. Por otra parte, los alcanos de cadena cerrada se llaman cicloalcanos. Además, la fórmula general de los n-alcanos es (CnH2n+2) y la fórmula general de los cicloalcanos es (CnH2n). (Esta fórmula es similar a la de algunos alquenos).
Nomenclatura de los alcanos
Los n-alcanos o alcanos de cadena lineal, se nombran de manera muy sencilla. Primero, se usa un prefijo que indica el número de carbonos en la molécula. Segundo, se añade el sufijo “ano”. La tabla 2 muestra varios ejemplos.
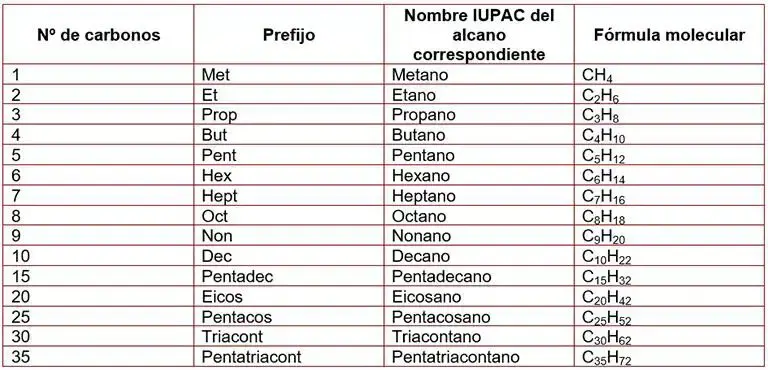
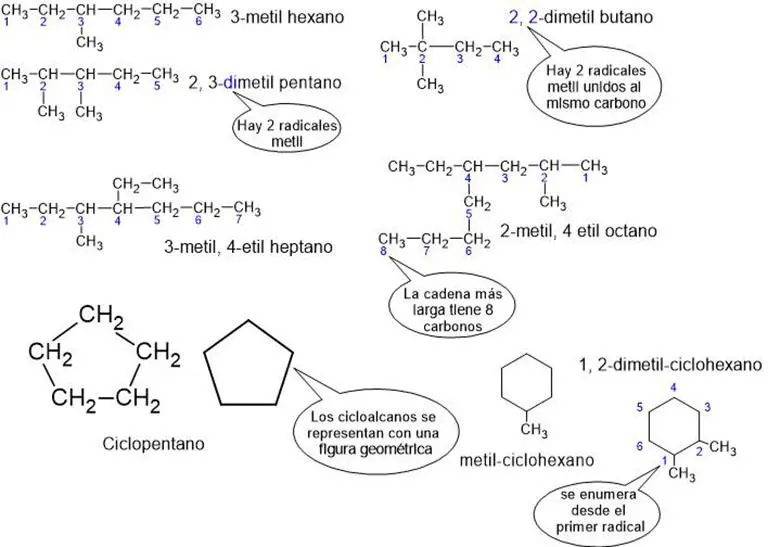
Para nombrar alcanos de cadena ramificada se siguen 3 pasos. Primero se determina la cadena de carbonos más larga de la molécula. Segundo, se enumeran los carbonos empezando por el extremo más cercano a la primera ramificación. Tercero, se nombran dichas ramificaciones colocando el número de carbono al cual está unida y se termina el nombre como en un n-alcano. Los nombres de los radicales que forman las ramificaciones tienen el prefijo que indica el número de carbonos y terminan en il. Por ejemplo, metil (CH3─), etil (C2H5─), propil (C3H7─), etc. Finalmente, si hay varias ramificaciones, se nombran en orden de complejidad (de menor a mayor número de carbonos).
Los cicloalcanos se nombran anteponiendo la palabra ciclo al nombre del n-alcano correspondiente. Además, para cicloalcanos con radicales o ramificaciones, se procede como en el caso de los alcanos ramificados de cadena abierta.
Ejemplos de nomenclatura de alcanos
Usos y aplicaciones de los alcanos
Los alcanos se usan principalmente como combustibles. Sin embargo, también se usan como materia prima en la síntesis de gran cantidad de compuestos orgánicos. Los primeros 4 de la serie, hacen parte del gas natural y se usan, entre otras cosas, como propelentes en distintas clases de aerosoles. El metano puede obtenerse por fermentación anaerobia de materiales orgánicos (es conocido como biogás)
Taller de lectura
- ¿Qué son los alcanos y por qué se les llama hidrocarburos saturados?
- Escriba el valor del ángulo entre los enlaces de un alcano y, además, las longitudes de dichos enlaces.
- ¿A qué equivale un Angstrom?
- Describa en qué consiste la hidrogenación de alquenos y, además, copie la reacción.
- ¿En qué consiste la reducción de halogenuros de alquilo?
- Describa la reacción de Wurtz y la hidrólisis del reactivo de Grignard. También, copie las reacciones.
- Haga un resumen de las propiedades físicas de los alcanos.
- Haga un resumen de las propiedades químicas de los alcanos y, además, copie cada una de las reacciones.
- ¿Cómo se clasifican los alcanos?
- Escriba como se nombran los n-alcanos y, también, copie la tabla 2.
- Escriba qué pasos se siguen para nombrar alcanos de cadena ramificada y, además, copie los 8 ejemplos de nomenclatura de alcanos.
- ¿Cuáles son los posibles usos de los alcanos?
