Termodinámica es la parte de la física que estudia los fenómenos relacionados con el calor. Concretamente, su transferencia de un cuerpo a otro y su conversión en energía mecánica. Esta disciplina debe su desarrollo a la necesidad de optimizar la eficiencia propia de las máquinas de vapor. Sin embargo, hoy se encarga del funcionamiento y rendimiento de los motores de combustión interna y otros sistemas físicos.
Sistemas físicos
Un sistema físico es un cuerpo o conjunto de cuerpos aislados físicamente o, solo idealmente, del resto del universo, con el fin de estudiarlo. Por otro lado, todo aquello que no pertenece al sistema, se llama vecindad. Además, un sistema puede interactuar con la vecindad de diferentes maneras. Existen 3 tipos de sistemas físicos:
Primero, Sistema aislado es aquel que no intercambia materia ni energía con la vecindad. Por ejemplo, el universo mismo es un sistema aislado.
Segundo, Sistema cerrado es el que intercambia energía (en forma de calor o trabajo) con la vecindad, pero no intercambia materia.
Además, un sistema abierto, es el que intercambia, tanto materia como energía con la vecindad. Cada uno de los seres vivos, por ejemplo, somos sistemas abiertos.
Primera ley de la termodinámica
La primera Ley de la termodinámica está relacionada con la conservación de la energía. La energía interna de un sistema (U), es la suma de las diversas formas de energía que poseen sus átomos y moléculas. Por otro lado, cuando el sistema interactúa con su vecindad, generalmente, intercambia energía. Puede absorber o liberar calor y efectuar o recibir trabajo. En consecuencia, su energía interna sufre variaciones y pasa de un estado inicial Ui, a otro final Uf. Entonces, la variación de la energía interna es:
ΔU = Uf – Ui
Al calor absorbido y el trabajo realizado por el sistema, son positivos. Por otro lado, el calor liberado y el trabajo realizado sobre el sistema, son negativos. En otras palabras, si un sistema absorbe una cantidad de calor Q y realiza un trabajo T, el principio de conservación de la energía, permite concluir que la variación de la energía interna del sistema, está dada por:
ΔU = Q – T
4 ejemplos cortos
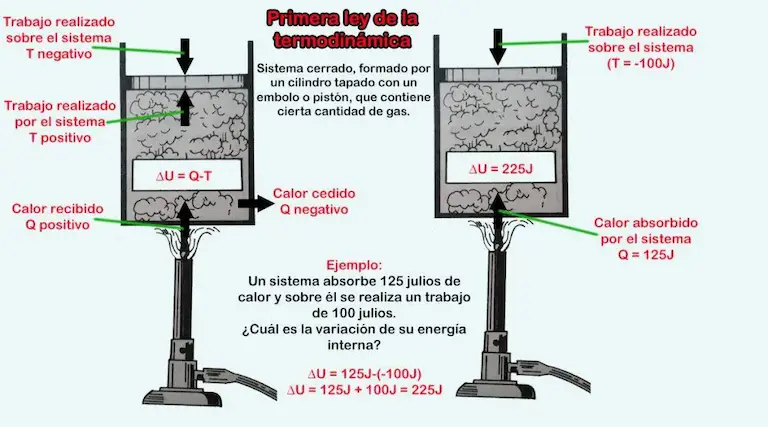
Para estos ejemplos, considere un sistema cerrado, formado por un cilindro tapado con un embolo o pistón, que contiene cierta cantidad de gas (Figura 1) y la ecuación (ΔU = Q – T).
Primero: El sistema absorbe 10 julios de calor y realiza un trabajo de 3 julios.
Solución: como el calor absorbido y el trabajo realizado, son positivos, la expresión queda:
ΔU = 10J – 3J
ΔU = 7J
El valor positivo indica que la energía interna del sistema aumentó en 7 julios.
Segundo: El sistema absorbe 125 julios de calor y sobre él se realiza un trabajo de 100 julios.
Solución: el calor absorbido es positivo, pero el trabajo realizado sobre el sistema es negativo, por lo tanto, la fórmula queda:
ΔU = 125J – (–100J)
ΔU = 125J + 100J = 225J
El valor positivo indica que la energía interna del sistema aumentó en 225 julios.
Tercero: El sistema libera 420 julios de calor y, a su vez, realiza un trabajo de 300 julios.
Solución: como el calor liberado es negativo, pero el trabajo realizado por el sistema es positivo, la fórmula queda:
ΔU = –420J – 300J
ΔU = –720J
El valor negativo indica que la energía interna del sistema disminuyó en 720 julios.
Cuarto: El sistema libera 200 julios de calor y sobre él se realiza un trabajo de 150 julios.
Solución: como el calor liberado es negativo, y el trabajo realizado sobre el sistema también es negativo, la fórmula queda:
ΔU = –200J – (–150J)
ΔU = –200J + 150J = –50J
El valor negativo indica que la energía interna del sistema disminuyó en 50 julios.
Segunda ley de la termodinámica
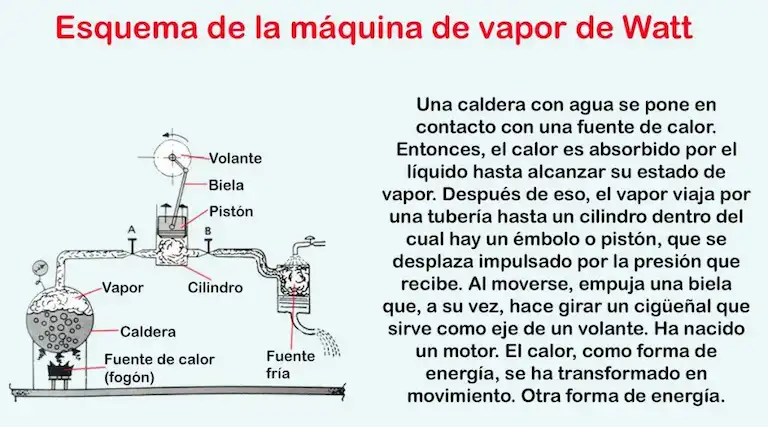
La segunda ley de la termodinámica señala que solo es posible la realización de un trabajo a partir del paso del calor de un cuerpo con mayor temperatura a uno de menor temperatura. Además, esta ley explica por qué una parte de la energía no puede convertirse en trabajo. En otras palabras, una máquina térmica retira cierta cantidad de calor Q1 de una fuente caliente. Por ejemplo, del fogón que calienta la caldera en la máquina de vapor de James Watt. La máquina emplea parte de ese calor para realizar trabajo T, y cede otra cantidad de calor Q2, a una fuente fría. El rendimiento R de la máquina está dado por la relación entre el trabajo que realiza y el calor que recibe en cada ciclo.
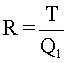
Teniendo en cuenta la fórmula de la primera ley de la termodinámica, el rendimiento puede escribirse como:
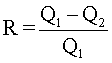
En la práctica, las máquinas térmicas más eficientes (los motores Diesel), alcanzan un rendimiento cercano al 50%. Es decir, ellas trasforman en trabajo, cerca de la mitad de la energía que obtienen del combustible.
Taller de lectura
- Escriba la definición de termodinámica.
- ¿De qué se encarga hoy la termodinámica?
- Escriba las definiciones de sistemas aislado, cerrado y abierto.
- ¿Qué dice la primera ley de la termodinámica?
- Escriba la fórmula para calcular la variación de la energía interna de un sistema.
- Copie los 4 ejemplos cortos.
- Describa la manera cómo funciona una máquina de vapor.
- ¿Quién construyó la máquina de vapor?
- ¿Qué dice la segunda ley de la termodinámica?
- Escriba las dos fórmulas para calcular el rendimiento de una máquina térmica.
