La normalidad es una unidad de concentración de las soluciones químicas. La normalidad de una solución se designa con la letra N. Se define como el número de equivalente gramo de soluto, contenidos en un litro de solución. La fórmula de la normalidad es:
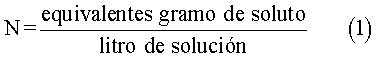
De acuerdo con la fórmula, las unidades de la normalidad son equivalente gramo sobre litro (eq-g/L).
¿Qué es un equivalente gramo?
Un equivalente gramo (eq-g) de un ácido, es la masa en gramos del ácido que puede producir un mol de hidrógeno H+. En la misma línea, un equivalente gramo de una base, es la masa en gramos de la base que puede producir un mol de OH–. El concepto de equivalente gramo se debe al químico alemán Karl Friedrich Wenzel.
Por lo general un equivalente gramo de un ácido o de una base se determina dividiendo la masa de un mol de compuesto entre el número de H+ u OH–. Por ejemplo, la masa molecular del ácido sulfúrico H2SO4 es 98 gr/mol. Al ver la fórmula. se observa que esta sustancia puede aportar 2 moles de H+. en consecuencia. La masa de un equivalente gramo de este ácido es de 49 gramos (98gr/mol dividido entre 2). Del mismo modo, la masa molecular del hidróxido de aluminio Al(OH)3 es 78gr/mol. Su fórmula muestra que puede aportar 3 moles de OH–. Entonces, la masa de un equivalente gramo de esta base es de 26 gramos (78gr/mol dividido entre 3). La tabla 1 muestra otros ejemplos.
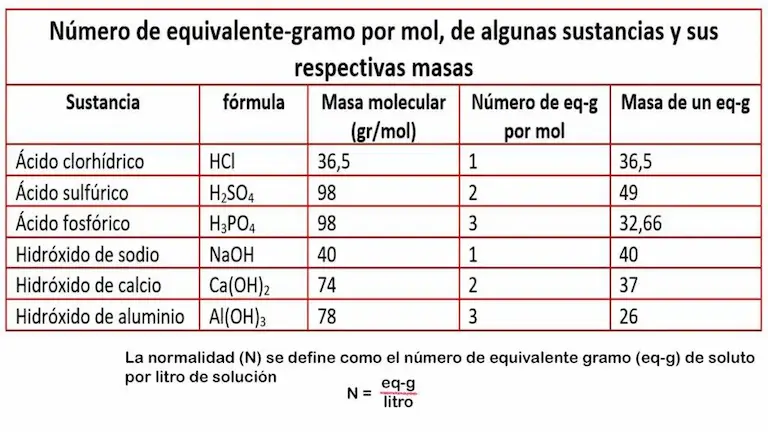
También, es posible calcular un equivalente gramo de una sal. Sin embargo, esto depende de la reacción y del empleo de la sal como base o ácido. Por lo tanto, puede ser variable. De todas maneras, un equivalente gramo de una sal, puede definirse como la masa en gramos de la sal que puede aportar un mol de iones negativos o positivos./p>
Importancia de la normalidad o concentración normal
Establecer la concentración de una solución en términos de normalidad es importante porque facilita los cálculos en 3 aspectos relacionados con las reacciones químicas.
Primero, en reacciones de oxido reducción, porque un equivalente gramo de agente reductor reacciona con un equivalente gramo de agente oxidante.
Segundo, en reacciones electroquímicas, porque un equivalente gramo del donador de electrones reacciona con un equivalente gramo del aceptor.
Tercero, en reacciones de neutralización o titulación, porque un equivalente gramo de base neutraliza un equivalente gramo de ácido.
Ejercicios resueltos de normalidad
Calculando la normalidad
ejercicio 1
¿Cuál es la normalidad de una solución de ácido sulfúrico (H2SO4) que tiene 24,5 gramos del ácido en 1500ml de solución? La masa molecular del ácido es 98gr/mol.
Procedimiento:
Primero, se determina el equivalente gramo presente en el soluto dado. Para esto, se multiplica la cantidad de soluto dada en gramos (gr) por el número de equivalente gramo presentes en un mol de soluto (eq/mol) y se divide entre la masa molecular del soluto (pm). En consecuencia, la fórmula para calcular el número de equivalente gramo presentes en una muestra de soluto es:
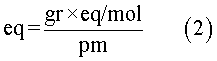
En este caso,
- gr = 24,5gr
- eq/mol = 2, porque el ácido puede producir 2 moles de H+.
- pm = 98 gr/mol
Al reemplazar los valores en la fórmula (2) se tiene:
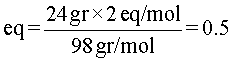
En resumen, la solución tiene 0,5 equivalente gramo.
Segundo, se representa el volumen en litros. Para esto se divide el volumen dado en mililitros entre mil. Por lo tanto, 1500ml equivalen a 1,5 litros (1500 se divide entre 1000).
Finalmente, se reemplazan los valores calculados en la fórmula de normalidad (1).
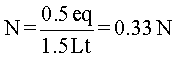
Por lo tanto, la normalidad de la solución dada es 0,33.
Preparando una solución normal a partir de soluto puro
ejercicio 2
Preparar 700 mililitros de una solución 0,3 normal de ácido fosfórico H3PO4. si su masa molecular es 98gr/mol.
Procedimiento:
Para preparar la solución es necesario saber cuantos gramos del ácido se necesitan. Para esto, se multiplican el volumen y la concentración requeridas por la masa de un equivalente gramo del ácido. Sin embargo, esta masa se halla dividiendo la masa molecular del soluto entre el número de moles de hidrógeno que puede aportar. En este caso, es 3. Entonces, se tiene:
- Volumen requerido 700ml = 0,7 litros.
- Concentración requerida = 0,3N o 0,3eq-g/litro.
- Masa molecular = 98gr/mol.
- Equivalente-g por mol = 3 porque el ácido puede ceder 3 moles de H+.
Por lo tanto, la cantidad de ácido que se necesita es:
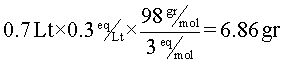
En resumen, para esta solución se necesitan 6,86 gramos de ácido fosfórico. Para terminar, se miden los 6,86 gramos del ácido, se vierten en un recipiente adecuado y se agrega agua hasta completar los 700 mililitros.
Preparando una solución normal a partir de otra solución
ejercicio 3
Preparar 450 mililitros de una solución 0,4N de hidróxido de sodio, a partir de una solución 0,6N.
Procedimiento:
Para este tipo de ejercicios se utiliza la fórmula:
V1 × N1 = V2 × N2 (3)
Sabiendo que V1 y N1, son el volumen y la concentración de la solución a preparar. Además, V2 y N2 son el volumen y la concentración de la solución que se va a utilizar. Por lo tanto, V2 es el valor a calcular. Entonces de la fórmula (3) se tiene:
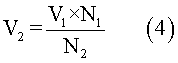
Se reemplazan los valores en la fórmula (4)
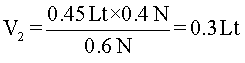
Según lo anterior, se requieren 0,3 litros (300ml) de la solución inicial. En consecuencia, se miden los 300 mililitros en un recipiente adecuado y se agrega agua hasta completar los 450 mililitros que se piden.
ejercicio 4
¿Cuál es la normalidad de una solución de ácido clorhídrico (HCl), si 25 mililitros de esta solución, neutralizan 20 mililitros de una solución 0,5 normal de hidróxido de sodio (NaOH)?
Procedimiento
La ecuación del proceso es:
HCl + NaOH → NaCl + H2O
Según la ecuación, se requiere un mol de HCl para neutralizar un mol de NaOH. Además, las dos sustancias tienen un equivalente gramo por mol (tabla 1). En consecuencia, la normalidad preguntada se puede hallar con la fórmula (3).
Donde N1 es la normalidad del HCl que se debe hallar y V1 es el volumen del HCl 25ml = 0,025 litros. Igualmente, N2 es la normalidad del NaOH = 0,5N y V2 es el volumen del NaOH 20ml = 0,020 litros.
Para terminar, se despeja N1 de la ecuación (3), se reemplazan los valores y se hacen las operaciones.
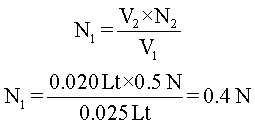
En conclusión, la normalidad de la solución de HCl es 0,4N
Taller de lectura
- ¿Cómo se define la normalidad?
- Escriba la fórmula de normalidad.
- ¿Qué es un equivalente gramo de un ácido y de una base?
- ¿Cómo se determina un equivalente gramo de un ácido o de una base? Escriba un ejemplo.
- ¿Cuál es la importancia de establecer la concentración de una solución en términos de normalidad?
- Copie, con los procedimientos, los ejercicios 1, 2, 3 y 4.
