La molalidad es una unidad de concentración de soluciones, que se define como el número de moles de soluto por kilogramo de solvente. Se representa con la letra m (minúscula). Matemáticamente se puede calcular dividiendo la cantidad de soluto en moles, entre la masa de disolvente en kilogramos.
Importancia de la molalidad
La molalidad es una herramienta útil para comprender las propiedades de las soluciones. La relación entre la molalidad y las propiedades coligativas, por ejemplo, es una de las aplicaciones más importantes de la química. Por otro lado, se utiliza con frecuencia para expresar la concentración de soluciones porque es independiente de la temperatura y la presión. En consecuencia, facilita el control de calidad en la industria alimentaria, la farmacología y la ingeniería química.
La molalidad y las propiedades coligativas
El uso de la molalidad como unidad de concentración, facilita el cálculo de las propiedades coligativas. Por ejemplo, el aumento del punto de ebullición y la disminución del punto de congelación. Sir Charles Blagden fue uno de los primeros en estudiar estas propiedades.
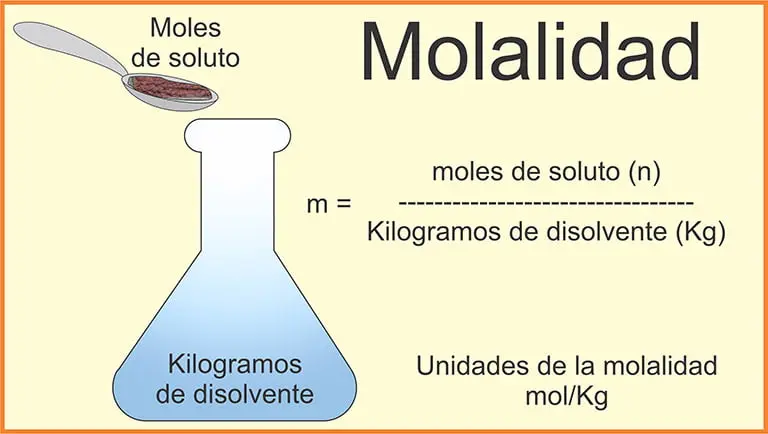
Fórmulas y ejercicios de aplicación
Como ya se anotó, la molalidad se calcula dividiendo la cantidad de soluto en moles, entre la masa de disolvente en kilogramos.
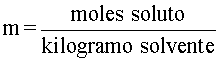
Sin embargo, de acuerdo con las preguntas planteadas, esta fórmula puede variar o aplicarse de formas diferentes. A continuación, se desarrollan algunos ejemplos.
Calculando la molalidad o concentración molal
Ejercicio 1
¿Cuál es la molalidad de una solución que se preparó con 0,2 moles de NaCl en 0,4 kilogramos de agua?
Solución: en este caso, simplemente se aplica la fórmula de la molalidad, porque el soluto está representado en moles y el solvente en kilogramos. Entonces,
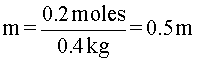
En resumen, la concentración de la solución es 0,5 molal.
Ejercicio 2
Calcular la concentración molal de una solución que se preparó con 40 gramos de glucosa C6H12O6, en 150 gramos de agua.
Solución: En este caso se debe hacer la conversión de gramos a moles de glucosa y la conversión de gramos a kilogramos de agua.
Para hallar los moles de glucosa, primero se calcula el peso molecular, sumando los pesos atómicos de los átomos que forman la molécula. Según la fórmula (C6H12O6), se multiplica el peso atómico del carbono (12,01) por 6. Además, el peso atómico del hidrógeno (1,008) por 12 y, finalmente, el peso atómico del oxígeno (15,99) por 6. Después de eso, se suman los resultados.
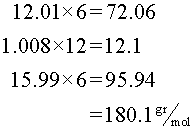
Es decir, el peso molecular de la glucosa es 180,1 gramos/mol.
Para calcular la cantidad en moles de glucosa, se divide la cantidad en gramos dada por el enunciado del ejercicio, entre el peso molecular.
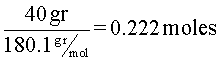
A continuación, se hace la conversión de gramos a kilogramos, sabiendo que 1Kg es igual a 1000gr
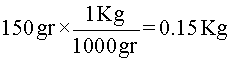
Finalmente, se aplica la fórmula de la concentración molal.
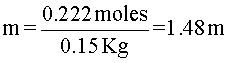
En conclusión, la concentración de la solución es 1,48 molal.
Calculando la cantidad de soluto necesario para preparar una solución molal
Ejercicio 3
¿Cuántos gramos de AgNO3 se necesitan para mezclar con 250ml de agua y preparar una solución 0,2m? El peso molecular del AgNO3 es 170gr/mol. Además, la densidad del agua es 1gr/ml.
Solución: en este caso, primero se calcula la masa de solvente en Kg. Según el dato de densidad, cada mililitro de agua tiene una masa de 1 gr. En consecuencia, los 250ml tienen una masa de 250gr. Para hacer la conversión a kilogramos, se sigue el procedimiento mostrado en el ejercicio 2. En otras palabras, la masa del solvente es de 0,25Kg.
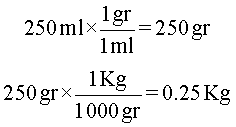
Segundo, se calcula el número de moles que debe haber en la solución que se va a preparar. Para esto, se multiplica la molalidad por la masa de disolvente. Se debe tener presente que las unidades de molalidad son mol/Kg.
0,2 mol/Kg × 0,25Kg = 0,05mol
Tercero, se hace la conversión de moles a gramos, multiplicando el número de moles por el peso molecular.
0,05 mol × 170gr/mol = 8,5gr
En conclusión, se necesitan 8,5 gramos de AgNO3, para preparar 250ml de una solución 0,2m.
Calculando la cantidad de soluto presente en una solución
Ejercicio 4
¿Cuántos gramos de etanol (C2H5OH) están disueltos en 325gr de agua, si la molalidad de la solución es 1,6m? El peso molecular del etanol es 46,1gr/mol.
Solución: Primero, se hace la conversión del disolvente de gramos a kilogramos.
La masa del agua en Kg es:
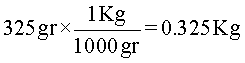
Segundo, se calcula la cantidad de etanol en moles, usando la fórmula de la molalidad. Para esto, se multiplica la concentración molal por la masa de agua en Kg.
La cantidad de etanol en moles es:
1,6 mol/Kg × 0,325Kg = 0,52 mol
Después de eso, se hace la conversión de moles a gramos del etanol. Esto se hace multiplicando la cantidad en moles por el peso molecular.
0,52 mol × 46,1gr/mol = 23,97gr
En resumen, en la solución hay 23,97 gramos de etanol disueltos.
Calculando la cantidad de disolvente
Ejercicio 5
Se requiere preparar una solución 0,45m a partir de 25gr de azúcar C12H22O11, cuyo peso molecular es 342,18gr/mol. ¿Cuál es la cantidad de agua que se requiere?
Primero, se hace la conversión del soluto de gramos a moles, dividiendo la cantidad en gramos entre el peso molecular.
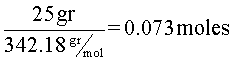
Después de eso, de la fórmula de molalidad, se despejan los kilogramos de disolvente, se reemplazan valores y se hacen las operaciones.
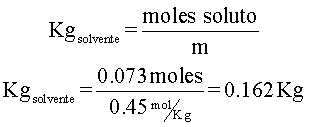
En conclusión, se requieren 0,162 kilogramos de agua para preparar la solución.
Taller de lectura
- Escriba la definición de molalidad, como se representa y, además, cómo se expresa matemáticamente.
- ¿Cuál es la importancia de la molalidad?
- ¿Qué relación hay entre la molalidad y las propiedades coligativas de las soluciones?
- Copie, con el procedimiento los 5 ejercicios resueltos de molalidad.
