Los números cuánticos son cantidades numéricas que describen las características de un electrón, en términos de su energía. Los números cuánticos son: principal, azimutal, magnético y spin.
Número cuántico principal (n)
El número cuántico principal se representa con n, y corresponde al nivel de energía en el que se encuentra un electrón. El valor de este número cuántico es un entero positivo. 1, 2, 3, 4, 5, 6 o 7. Además pueden nombrarse con las letras K, L, M, N, O, P y Q.
¿Cuántos electrones pueden acomodarse en un nivel de energía?
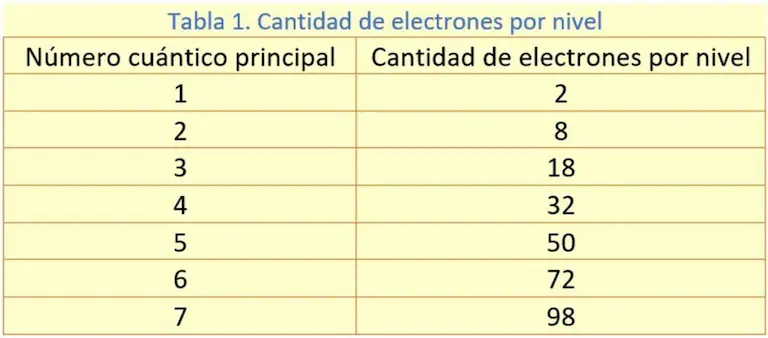
La cantidad de electrones en un nivel de energía, está dada por la fórmula 2n2, donde n es el número cuántico principal. La tabla 1 muestra la cantidad de electrones por nivel.
Número cuántico azimutal (l)
El número cuántico azimutal corresponde a lo que llamamos subniveles de energía. Puede identificarse con las letras s, p, d y f. Sin embargo, numéricamente toman valores desde cero hasta n-1. En otras palabras, en el nivel 1, está el subnivel cero (s); en el nivel 2, están los subniveles cero y uno (s y p); y así sucesivamente. Por otro lado, la cantidad de electrones por subnivel está limitada a 2 para el subnivel s; 6 para el p; 10 para el d; y 14 para el f. La tabla 2, muestra la relación entre el número cuántico principal y el azimutal. Es decir, la cantidad de subniveles por nivel de energía.

Nota aclaratoria: Aunque la teoría dice que tanto el número principal como el azimutal pueden ir hasta «infinito», en los átomos conocidos, los niveles van de 1 a 7 y los subniveles de 0 a 3 (de s a f).
Número cuántico magnético (m)
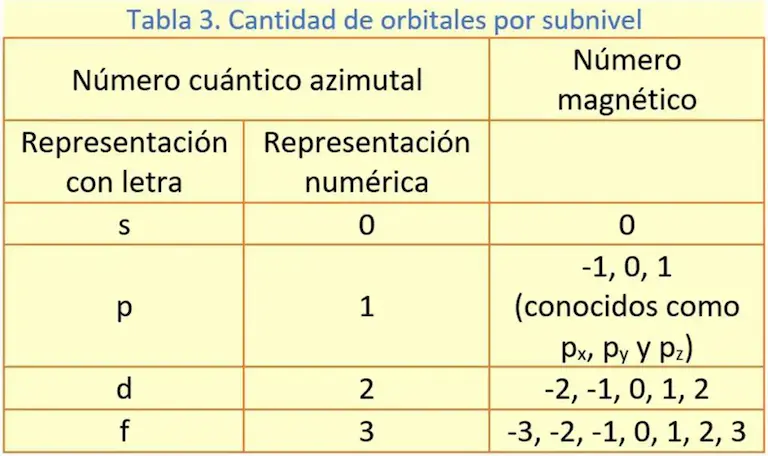
El número cuántico magnético, es lo que conocemos con el nombre de orbitales. Un orbital, es una región cerca al núcleo, donde es más probable encontrar un electrón. Se enumeran desde –l hasta +l. En cada orbital se acomodan máximo 2 electrones. La tabla 3, muestra la relación entre el número azimutal y el magnético.
Número cuántico spin (ms)
El número cuántico spin, solo puede tomar dos valores -½ ó +½. Un experimento realizado por Otto Stern en 1921, demostró que un electrón actúa como si pudiese girar en una de dos direcciones opuestas. El principio de exclusión de Pauli, dice que dos electrones pueden ocupar un mismo orbital, solo si giran en direcciones opuestas. Es decir, si uno tiene spin -½ y el otro +½. A un par de electrones así, se les llama antiparalelos.
Configuración electrónica
La configuración electrónica, es la forma específica de ocupación de los orbitales de un átomo, por parte de los electrones.
Para determinar la configuración electrónica de un átomo, en su estado fundamental, se sigue la regla del Aufbau. Según esta regla, los electrones se añaden al diagrama de ocupación, partiendo del primer nivel y, además, ocupando los niveles de energía más bajos, disponibles para ellos. El diagrama de ocupación se muestra en la figura 1.

La otra manera de determinar la organización de los electrones en un átomo, es con el diagrama de orbitales. En este diagrama, el número cuántico principal se representa con su valor numérico, el azimutal con su respectiva letra, el magnético u orbital con una línea sobre los dos anteriores y el spin con una semiflecha hacia arriba o hacia abajo. Además, la regla de Hund, dice que los electrones tienen a permanecer desapareados. Es decir, ubicando uno en cada orbital disponible, en el mismo subnivel, antes de colocar un segundo electrón. Por ejemplo, para el carbono con Z=6, el diagrama de orbitales es:
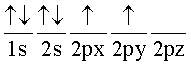
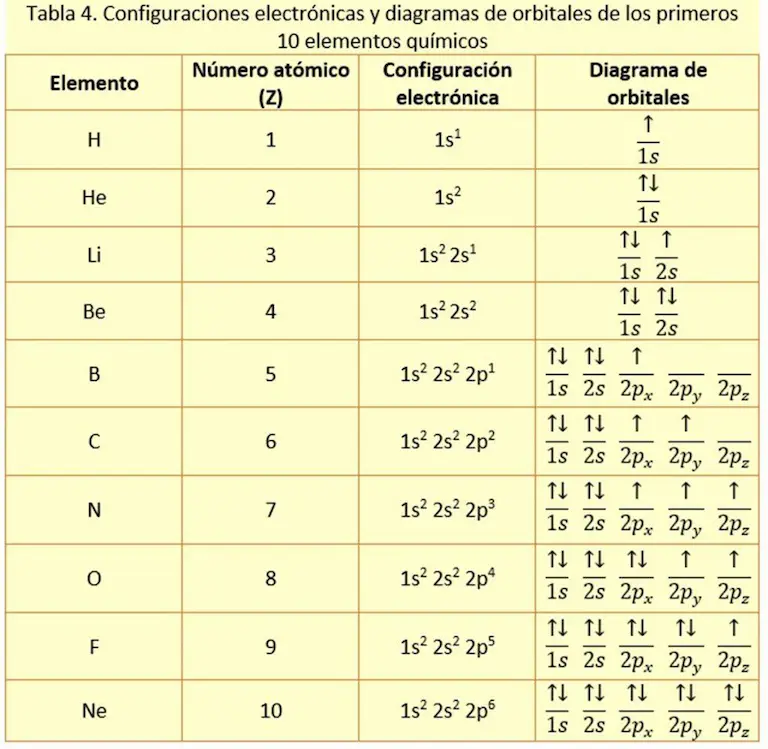
Este diagrama indica que en el primer nivel hay un subnivel s con 2 electrones; en el nivel 2 hay un subnivel s con 2 electrones; además, hay un electrón en el orbital px o -1, y un electrón en el orbital py o 0. También, hay un orbital pz o 1, que está vacío. La tabla 4 muestra la configuración electrónica y el diagrama de orbitales, de los primeros 10 elementos de la tabla periódica.
Taller de lectura
- ¿Qué son los números cuánticos?
- Complete la siguiente tabla:
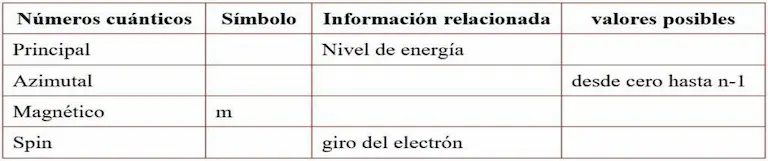
- ¿Cuántos electrones caben: primero, en cada nivel. Segundo, en cada subnivel. tercero, en cada orbital?
- ¿Qué es un orbital?
- ¿Qué es configuración electrónica?
- Copie la figura 1, con el diagrama de ocupación de orbitales.
- Describa la manera como se representan los números cuánticos en un diagrama de orbitales.
- Copie la tabla 4 con las configuraciones electrónicas y los diagramas de orbitales, de los 10 primeros elementos.
