La ley de las proporciones múltiples dice que cuando se combinan dos o más elementos en distintas proporciones, se forman compuestos también diferentes. Esta ley fue enunciada por John Dalton.
Por ejemplo, si se combinan carbono (C) y oxígeno (O) en proporción 1:2 (se lee uno a dos), se obtiene dióxido de carbono (CO2). La molécula tiene un átomo de carbono y dos átomos de oxígeno.
Sin embargo, cuando se combinan los mismos elementos pero en proporción 1:1, se obtiene monóxido de carbono (CO). Esta molécula tiene un átomo de carbono y un átomo de oxígeno.
Aunque los dos compuestos están formados por los mismos elementos, tienen propiedades totalmente diferentes. Mientras el CO2 es inocuo (inofensivo), el CO es altamente tóxico. neutraliza la hemoglobina evitando la fijación de oxígeno y produciendo muerte por asfixia.
La ley de las proporciones múltiples explica por qué existe una enorme cantidad de compuestos formados a partir de unos pocos elementos.
La tabla 1 muestra como a partir de cloro (Cl) y oxígeno (O) se obtienen 4 óxidos, variando la proporción en la que se combinan.
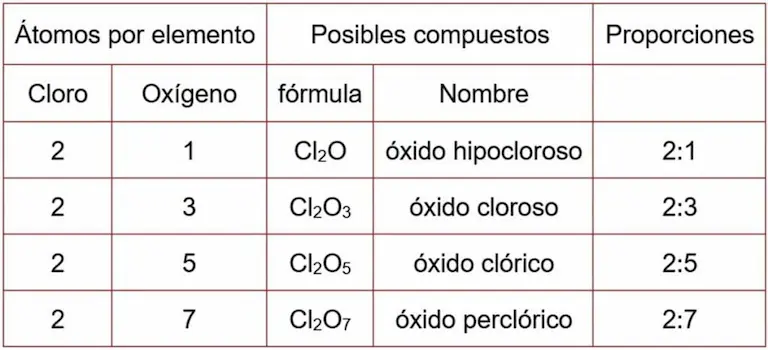
La cantidad de átomos en cada compuesto se indica con subíndices enteros, tal como muestra la tabla (columna fórmula).
Es necesario aclarar, que las proporciones en las que se puede combinar un átomo con otro, están determinadas por las valencias de cada átomo. La tabla 1, muestra que el oxígeno tiene, en estos compuestos, valencia dos, mientras el cloro tiene valencias 1, 3, 5, y 7.
Números de valencia
La valencia significa la capacidad de combinación de un átomo. Los electrones de la última capa, llamada por cierto, capa de valencia, son responsables de la formación de enlaces entre los átomos.
Podemos imaginar la valencia de un átomo, como la cantidad de manos que tiene para unirse a otros, en un compuesto dado. En las figuras 1 y 2 se muestra como el cloro puede unirse con el oxígeno, usando cada una de sus valencias.
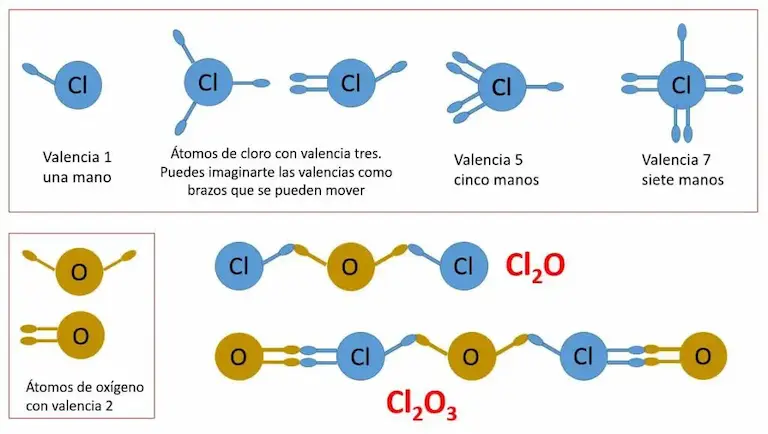
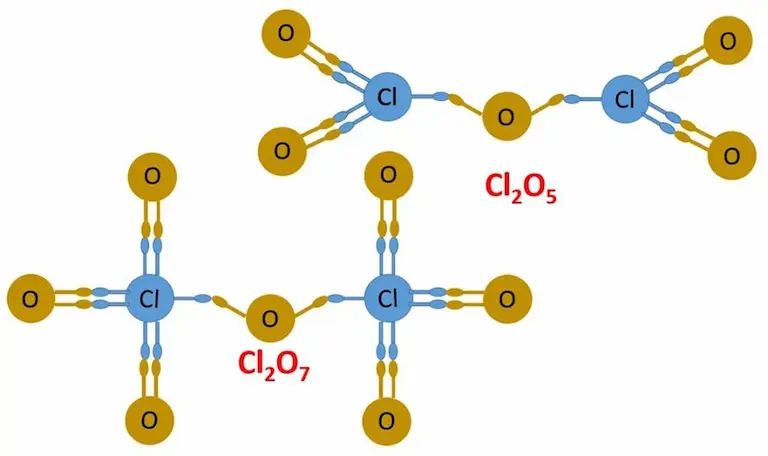
Numero de valencia y tabla periódica
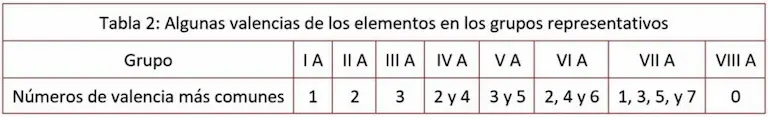
Los átomos de cada uno de los elementos químicos, tienen sus propias valencias, relacionadas generalmente con el grupo al cual pertenecen. Aunque podríamos ver la tabla periódica para identificarlas, también es posible deducirlas, ya que, por lo menos en los grupos A, ellas coinciden con el número del grupo y sus pares o impares menores. Por ejemplo, el carbono ubicado en el grupo IV A, tiene valencia 4 y 2. la primera es el número del grupo, que en este caso es par y la segunda es el par menor. Desde luego hay excepciones, pero esta es una buena generalización para empezar a entender este concepto. ¿Puedes deducir las posibles valencias del nitrógeno ubicado en el grupo VA? Muy bien! 5 y 3 son las principales. La tabla 2 muestra algunas valencias de los elementos en los grupos representativos (grupos A).
Taller de lectura
- ¿Qué dice la ley de las proporciones múltiples y quién la enunció?
- ¿Qué explica la ley de las proporciones múltiples?
- Copie la tabla 1.
- ¿Cómo se indica la cantidad de átomos en cada compuesto?
- ¿Qué de termina las proporciones en las que se puede combinar un átomo con otro?
- ¿De qué son responsables los electrones de la última capa en los átomos?
- ¿Cómo podemos imaginar la valencia de un átomo?
- Copie las figuras 1 y 2.
- Copie la tabla 2.
- De acuerdo con la lectura y las figuras 1 y 2, Dibuje y escriba las fórmulas de las moléculas formadas por átomos de oxígeno con valencia 2 y átomos de nitrógeno con valencias 3 y 5.
