Las fórmulas empíricas y moleculares, junto con las estructurales, brindan información acerca de la conformación de las moléculas.
Fórmulas empíricas
Las fórmulas empíricas o fórmulas mínimas, son aquellas que muestran la relación en la que se encuentran los átomos de los distintos elementos en un compuesto. Estas fórmulas no indican cuantos átomos hay en la molécula. Tampoco, la manera como se hallan agrupados en ella.
¿Cómo los químicos obtienen las fórmulas empíricas?
La palabra «empírico» señala que algo está basado en la práctica, la experiencia y la observación. En consecuencia, una fórmula empírica resulta del análisis, en laboratorio, de una muestra de materia.
Suponga que usted es químico y recibe en su laboratorio una muestra de materia para obtener su fórmula. Primero, debe establecer que se trata de una sustancia y no de una mezcla. Segundo, debe hacer pruebas para saber qué elementos químicos contiene (análisis cualitativo). Tercero, debe establecer la composición porcentual de esos elementos en la muestra (análisis cuantitativo). Finalmente, la fórmula empírica se calcula a partir de la composición porcentual de los elementos en el compuesto.
Procesos como este hacen parte de la química analítica, cuyo pionero fue Carl Remigius Fresenius.
¿Cómo se calculan las fórmulas empíricas?
Para calcular una fórmula empírica se siguen tres pasos:
Primero, se dividen los porcentajes de cada elemento, entre su peso atómico respectivo.
Segundo, los cocientes resultantes se dividen por el menor de ellos, y los resultados se aproximan al entero más cercano. Estos valores serán los subíndices de los elementos.
Tercero, se escriben los símbolos de los elementos con su respectivo subíndice. Sin embargo, recuerde que estos subíndices no indican la cantidad total de átomos en la molécula, sino su cantidad relativa.
Ejercicios resueltos de fórmulas empíricas
Ejercicio 1.
Hallar la fórmula empírica de una sustancia formada por 11.11% de hidrógeno y 88.89% de oxígeno.
Solución: Los datos se resumen en la siguiente tabla:
| Elemento | Porcentaje | Peso atómico |
|---|---|---|
| Hidrógeno | 11.11 | 1 |
| Oxígeno | 88.89 | 16 |
Procedimiento: Primero, se dividen los porcentajes entre los pesos atómicos:
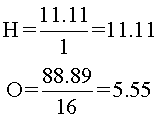
Después de eso, los cocientes (resultados de las divisiones), se dividen entre el menor de ellos:
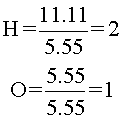
El subíndice del hidrógeno es 2 y el del oxígeno es 1. Es decir, en esta molécula, por cada 2 átomos de hidrógeno, hay 1 de oxígeno (2:1). Por lo tanto, la fórmula empírica es:
(H2O)n
Las fórmulas empíricas, normalmente se escriben entre paréntesis porque la relación calculada puede repetirse más de una vez en la molécula. En otras palabras, la fórmula anterior puede escribirse (H2O)n. Donde n indica la cantidad de veces que se repite la relación. Por lo tanto, si n es 1, las fórmulas empírica y molecular serían iguales. Por ejemplo, la fórmula empírica del agua es igual a su fórmula molecular.
Ejercicio 2:
Hallar la fórmula empírica de un compuesto formado 30% de oxígeno y 70% de hierro.
Solución: Los datos se resumen en la siguiente tabla:
| Elemento | Porcentaje | Peso atómico |
|---|---|---|
| Oxígeno | 30% | 16 |
| Hierro | 70% | 56 |
Procedimiento: Primero, se dividen los porcentajes entre los pesos atómicos:
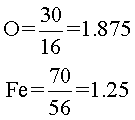
Posteriormente, los cocientes (resultados de las divisiones), se dividen entre el menor de ellos:
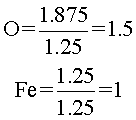
Nota: Cuando uno de los cocientes está cercano a las 5 décimas, como en este caso el oxígeno (1.5), la manera de obtener los subíndices es multiplicando por 2, todos los resultados. En consecuencia, el subíndice del oxígeno es 1.5×2=3 y el subíndice del hierro es 1×2=2. Es decir, la relación de átomos de hierro y oxígeno en la molécula es (2:3). En conclusión, la fórmula empírica buscada es:
(Fe2O3)n
Ejercicio 3
El análisis cuantitativo de una sustancia orgánica, revela que contiene 65% de carbono, 3,51% de hidrógeno, 21,91% de oxígeno y 9,58% de nitrógeno. ¿Cuál es su fórmula empírica?
Solución. En la siguiente tabla se resume el procedimiento, de tres pasos, propuesto anteriormente.
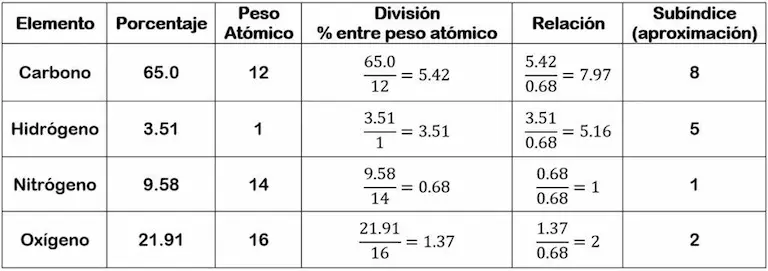
La tabla anterior indica que el subíndice del carbono es 8, el del hidrógeno 5, el del nitrógeno 1 y el del oxígeno 2. Por lo tanto, la fórmula empírica del compuesto es:
(C8H5NO2)n
Observe que el subíndice 1, del nitrógeno, no se escribe.
Fórmulas moleculares
Las fórmulas moleculares son aquellas que muestran, además de la relación y naturaleza de los átomos que forman la molécula, el número de átomos que contiene. Sin embargo, no establecen la manera como ellos se agrupan.
¿Cómo se calculan las fórmulas moleculares?
Las fórmulas moleculares, también pueden calcularse a partir de la composición porcentual. Pero, además, debe conocerse el peso molecular. Dicho cálculo puede hacerse en 3 pasos:
Primero, se representan los porcentajes dados, en gramos. Para esto, se usa la fórmula:
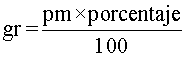
Donde pm, es el peso molecular y porcentaje, es el porcentaje de cada elemento.
Segundo, cada cantidad en gramos se divide entre el peso atómico respectivo.
Tercero, los cocientes se aproximan al entero más próximo y estos serán los subíndices.
Ejercicios resueltos de fórmulas moleculares
Ejercicio 4
El análisis de una sustancia indica que contiene 40% de carbono, 6.66% de hidrógeno y 53.33% de oxígeno. Hallar su fórmula molecular, sabiendo que el peso molecular es de 180 gr/mol.
Solución: Los datos se resumen en la siguiente tabla.
| Elemento | Porcentaje | Peso atómico |
|---|---|---|
| Carbono | 40% | 12 |
| Hidrógeno | 6.66% | 1 |
| Oxígeno | 53.33% | 16 |
Primero, se hallan las cantidades en gramos.
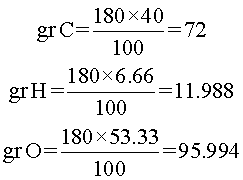
Después de eso, se hallan los subíndices, dividiendo los gramos de cada elemento entre su peso atómico. Además, se aproxima al entero más cercano.
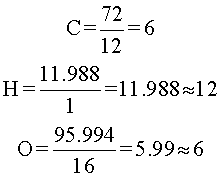
Es decir, el subíndice del carbono es 6, el del hidrógeno es 12 y el del oxígeno es 6. En consecuencia, la fórmula molecular del compuesto es
C6H12O6
Ejercicio 5
Se dice que la vitamina C (ácido ascórbico) tiene peso molecular de 176 gr/mol. Además, su composición porcentual es 40.9% de carbono, 4.54% de hidrógeno y 54.54% de oxígeno. Hallar su fórmula molecular.
Solución: Los datos se resumen en la siguiente tabla.
| Elemento | Porcentaje | Peso atómico |
|---|---|---|
| Carbono | 40.9% | 12 |
| Hidrógeno | 4.54% | 1 |
| Oxígeno | 54.54% | 16 |
Primero, se representan las cantidades en gramos.
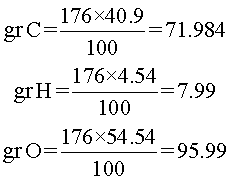
A continuación, se divide cada elemento entre su peso atómico respectivo.
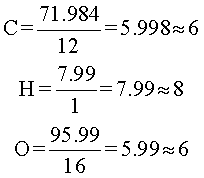
Entonces, el subíndice del carbono es 6, el del hidrógeno es 8 y el del oxígeno es 6. En conclusión, la fórmula molecular de la vitamina C, es:
C6H8O6
Un ejercicio más (Video)
Taller de lectura
- ¿Qué son las fórmulas empíricas?
- ¿Cómo los químicos obtienen las fórmulas empíricas?
- ¿Cómo se calculan las fórmulas empíricas?
- Copie, con los procedimientos, los ejercicios 1, 2 y 3.
- ¿Qué son las fórmulas moleculares?
- ¿Cómo se calculan las fórmulas moleculares?
- Copie, con los procedimientos, los ejercicios 4 y 5.
- Realice el siguiente ejercicio: Un compuesto orgánico está formado por carbono 92.3% e hidrógeno 7.69%. ¿Cuál es su fórmula empírica? Sabiendo que su peso molecular es 78 gr/mol ¿Cuál es su fórmula molecular?
