Enlace químico, es la fuerza que mantiene unidos los átomos que forman una molécula. Esta fuerza es de carácter eléctrico y en ella intervienen algunos electrones. Para entender el concepto de enlace químico, es necesario conocer los conceptos de electrones de valencia, regla del octeto y estructuras de Lewis. Más adelante, en las figuras 5, 6, 7 y 8, se muestran varios ejemplos de enlace químico.
Electrones de valencia
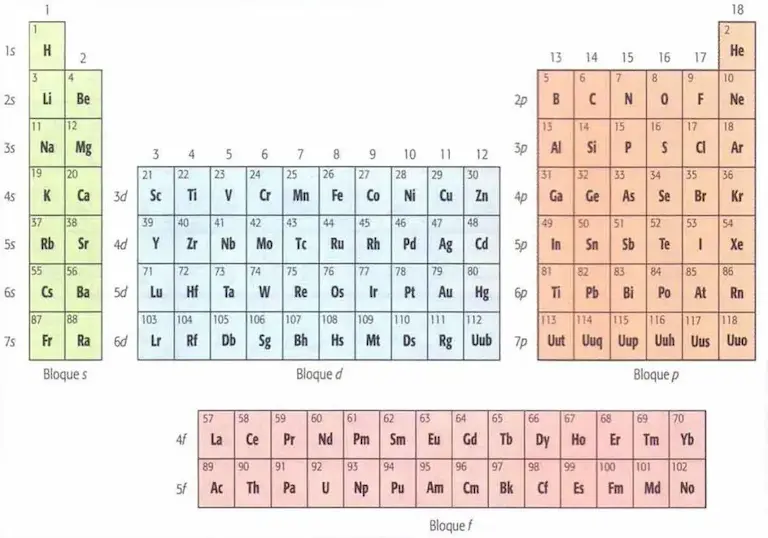
Los electrones de valencia son aquellos electrones que participan en la formación de un enlace. Están ubicados en el nivel externo de los átomos. En los metales alcalinos y alcalino térreos, estos electrones pertenecen al orbital s. Así mismo, en los elementos de los grupos IIIA a VIIA (grupos 13 a 17 en la notación actual), los electrones de valencia pertenecen al sub nivel p. Además, en los llamados elementos de transición, esos electrones están en el subnivel d. Finalmente, los elementos del bloque de tierras raras (lantánidos y actínidos), tienen sus electrones de valencia en un subnivel f. La figura 1 muestra esta distribución.
En resumen, ¿Cómo se forman los enlaces químicos? Los enlaces químicos se forman, cuando los átomos que se unen, comparten o transfieren entre sí, electrones de valencia para lograr configuraciones más estables.
La tabla 1, muestra la cantidad de electrones de valencia, en algunos grupos de la tabla periódica.
| Grupo | # de Electrones de valencia |
| 1 o IA | 1 |
| 2 o IIA | 2 |
| 13 o IIIA | 3 |
| 14 o IVA | 4 |
| 15 o VA | 5 |
| 16 o VIA | 6 |
| 17 o VIIA | 7 |
Regla del octeto
La regla del octeto establece que, en un enlace químico, los átomos pierden, ganan o comparten electrones para lograr una estructura electrónica estable. Es decir, la estabilidad se logra, cuando los átomos completan 8 electrones en su nivel de valencia (nivel externo). Esta configuración, entonces, es similar a la de los gases nobles.
Representaciones de Lewis
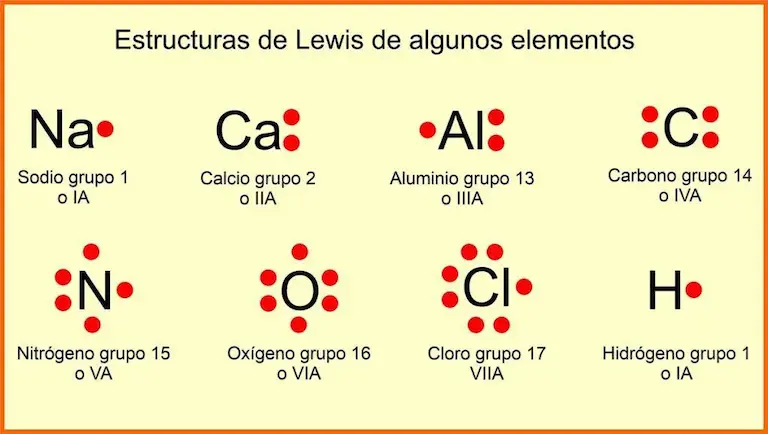
Son diagramas que permiten “visualizar” los electrones de valencia de un átomo. En las estructuras de Lewis, los electrones de valencia se indican por medio de puntos o cruces alrededor del símbolo del elemento. Además, el símbolo representa el núcleo y los electrones de los niveles internos del átomo. Estas estructuras sirven para representar los enlaces químicos. La figura 2, muestra algunos ejemplos.
Tipos de enlace químico
¿Cuántos tipos de enlace químico existen?
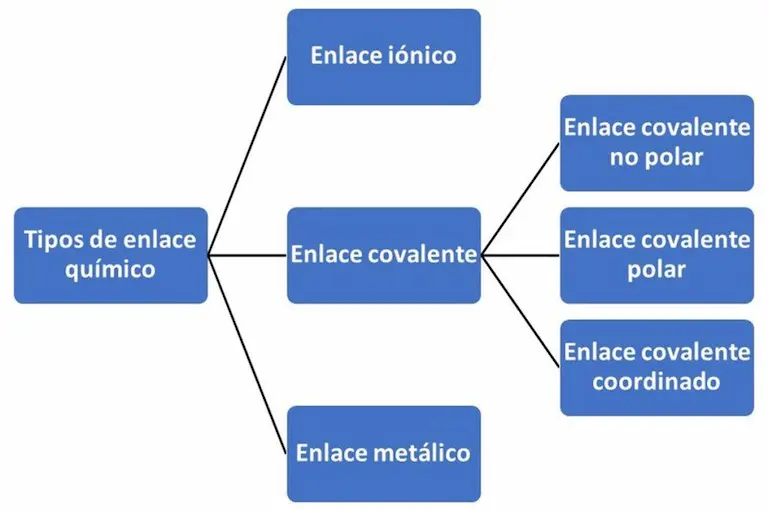
Existen 3 tipos de enlace químico: enlace iónico, enlace covalente (que puede ser polar, no polar o coordinado) y enlace metálico. La figura 3, muestra un mapa conceptual de las clases de enlaces químicos.
Enlace iónico
Enlace iónico es aquel en el cual hay transferencia completa de electrones de un átomo a otro. El átomo que pierde electrones se transforma en un ion positivo llamado catión. Por el contrario, el átomo que acepta los electrones forma un ion negativo que se denomina anión. A la cantidad de electrones perdidos o ganados, se le llama número de oxidación. Los elementos metálicos tienden a ceder electrones, mientras los elementos No-metales, tienden a recibirlos. Sin embargo, la cantidad de electrones recibidos (cargas negativas), debe ser igual a la cantidad de electrones cedidos (cargas positivas). Una de las propiedades que determina estos comportamientos es la electronegatividad (EN).
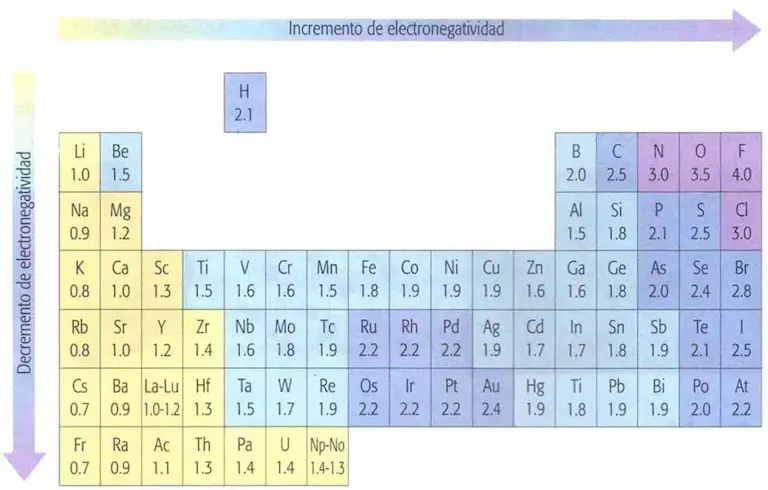
La electronegatividad es la capacidad de un átomo para atraer los electrones involucrados en un enlace. Un enlace se considera iónico, cuando la diferencia entre las electronegatividades de los átomos que lo forman es mayor o igual a 1,7. La figura 4, muestra la electronegatividad de algunos elementos.
propiedades de los enlaces iónicos
Los enlaces iónicos tienen 2 características principales:
Por un lado, los enlaces iónicos forman compuestos que tienen puntos de fusión y ebullición altos, comparados con compuestos formados por enlaces covalentes.
Por otro lado, los compuestos formados por enlaces iónicos son solubles en agua y se disocian en la solución, liberando los iones que los componen. Una sustancia que produce iones en solución acuosa se llama electrolito. Además, las soluciones de estas sustancias permiten el paso de la electricidad.
Ejemplos de enlace iónico
La figura 5, muestra 4 ejemplos de enlaces iónicos, que se explican a continuación.
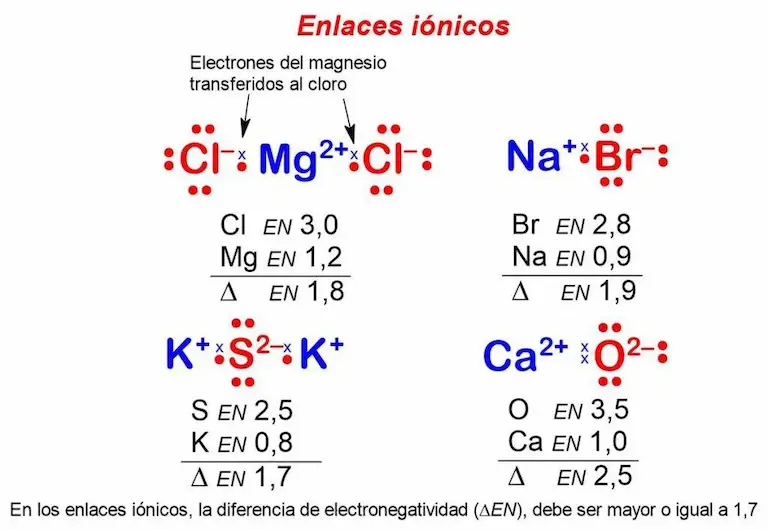
En el primer ejemplo, se requieren 2 átomos de cloro para combinarse con uno de magnesio. ¿por qué? Porque el cloro tiene 7 electrones de valencia y solo requiere de uno para completar 8 y cumplir con la regla del octeto. Por su parte, el magnesio debe ceder sus 2 electrones de valencia. En consecuencia, cede uno a cada cloro. Los electrones de valencia del cloro se representan con puntos y los del magnesio con x. el signo negativo en los átomos de cloro indica que han recibido un electrón. Del mismo modo, el 2+ en el magnesio, indica que ha cedido 2 electrones. En otras palabras, el cloro formó aniones y el magnesio formó un catión. Los valores numéricos, en la figura, representan la diferencia de electronegatividad entre los elementos involucrados en el enlace.
En el segundo ejemplo, el bromo tiene 7 electrones de valencia y debe recibir uno para completar sus 8. El sodio, por su parte, tiene un electrón que puede ser transferido al bromo.
En el tercer ejemplo, el azufre requiere de 2 electrones para completar 8 pero el potasio solo puede aportar uno, por esa razón, se necesitan dos átomos de potasio para combinarse con uno de azufre.
Finalmente, en el cuarto ejemplo se requiere un átomo de oxígeno para combinarse con uno de calcio. El oxígeno tiene 6 electrones de valencia y, para completar 8, acepta los 2 que tiene para ceder el calcio.
Enlace covalente
El enlace covalente es aquel que se forma cuando los átomos comparten algunos electrones de valencia, de manera que cumplan con la regla del octeto. Los electrones compartidos forman orbitales moleculares que pasan más tiempo alrededor del átomo más electronegativo formando polos o cargas parciales. Estas se representan con la letra delta minúscula (δ). Además, los enlaces covalentes pueden ser simples, dobles o triples, si comparten uno, dos o tres pares de electrones respectivamente. Generalmente, estos enlaces se representan con una, dos o tres líneas. Las figuras 6 y 7 muestran algunos ejemplos.
Propiedades de los enlaces covalentes
Una particularidad de este tipo de enlace, es que puede formarse entre átomos del mismo elemento. Por otro lado, los compuestos formados por enlaces covalentes tienden a ser insolubles en agua y los que son solubles, no forman electrolitos. En consecuencia, dichas soluciones no dejan pasar la electricidad. Adicionalmente, los compuestos formados por enlaces covalentes, tienen puntos de fusión y ebullición menores que los compuestos iónicos.
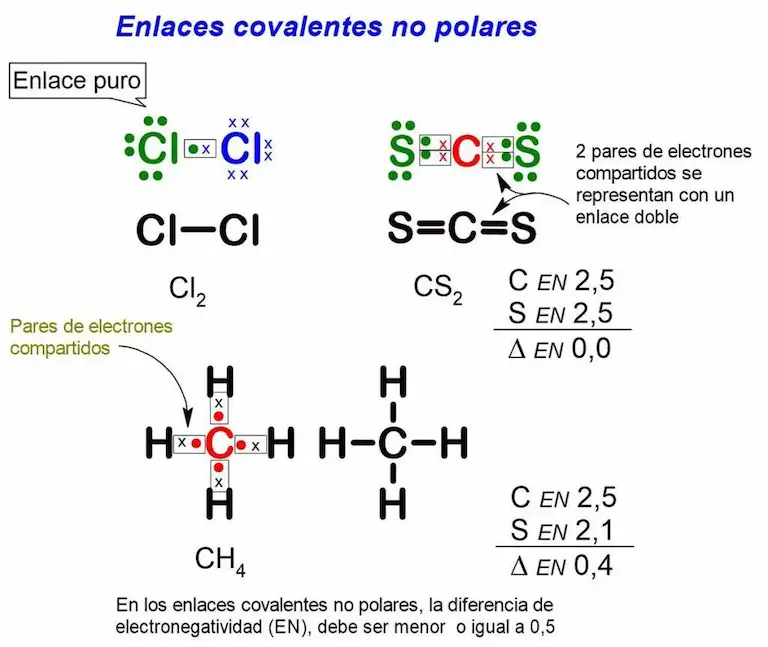
Enlace covalente no polar
Un enlace covalente no polar, es aquel que se forma entre átomos cuyas cargas eléctricas negativas se distribuyen por igual o casi por igual. Un enlace se considera no polar, cuando la diferencia de electronegatividades es igual o menor a 0,5. Por ejemplo, en el CS2, tanto el azufre como el carbono tienen electronegatividad de 2,5 (ver figura 4). Es decir, la diferencia de electronegatividades es cero. Por otra parte, un enlace covalente puro, es un enlace covalente no polar que se forma entre átomos del mismo elemento.
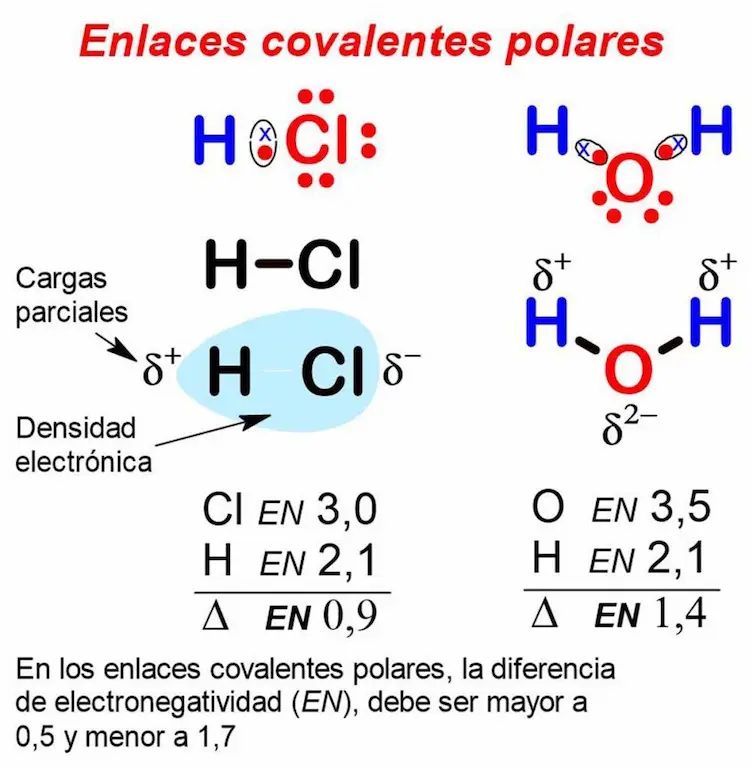
Enlace covalente polar
Un enlace covalente polar, es aquel que se forma entre átomos cuyas cargas eléctricas negativas se no distribuyen por igual. En otras palabras, la mayor densidad de cargas eléctricas negativas permanece alrededor del elemento más electronegativo. En consecuencia, se forman un polo positivo (δ+) y un polo negativo (δ─). Sin embargo, la diferencia de electronegatividad es menor que en los enlaces iónicos. Por lo tanto, la diferencia de electronegatividad entre los átomos es un enlace covalente polar, es menor a 1,7 y mayor que 0,5. Por ejemplo, en el enlace químico del agua, la diferencia de electronegatividad es de 1,4.
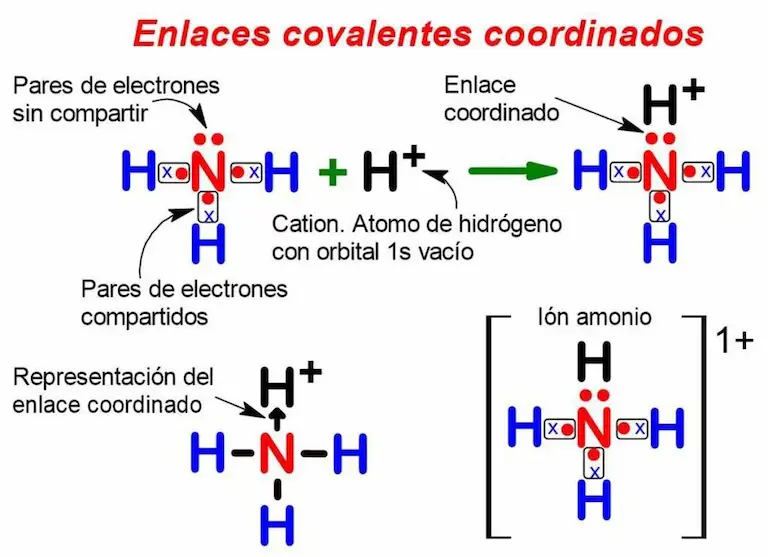
Enlace covalente coordinado
El enlace covalente coordinado, es aquel en el que los electrones necesarios para formar el enlace, son aportados por uno solo de los átomos. Por un lado, el átomo que proporciona los electrones, debe tener al menos un par no compartido en su nivel de valencia. Por otro lado, el átomo que recibe los electrones, debe necesitarlos para lograr su configuración estable (regla del octeto). Además, un enlace coordinado se representa con una flecha que apunta hacia el átomo que acepta los electrones.
Enlace químico tipo metálico
Se forma entre átomos de elementos metálicos. En este tipo de enlace, los electrones de valencia de varios átomos, se mueven libremente cerca de los núcleos. En otras palabras, los electrones de valencia no están localizados en una posición definida, sino que gozan de gran movilidad. Dicha movilidad explica algunas características de los metales, como, Por ejemplo, la conductividad eléctrica y térmica.
Taller de lectura
- ¿A qué se le llama enlace químico?
- ¿Cuáles son los electrones que participan en un enlace químico?
- Copie la tabla que muestra la cantidad de electrones de valencia, en algunos grupos de la tabla periódica.
- ¿En qué consiste la regla del octeto y qué logran los átomos con esto?
- ¿Qué son las representaciones de Lewis y cómo se indican los electrones de valencia en esas representaciones?
- Copie la figura 2.
- Copie el mapa conceptual de las clases de enlaces químicos.
- ¿Qué es un enlace iónico?
- ¿Cómo se llama un átomo que pierde electrones y uno que los gana?
- ¿Qué es número de oxidación?
- ¿Qué tipo de elementos tiende a ceder electrones y qué tipo tiende a recibirlos?
- Escriba la definición de electronegatividad.
- ¿Cuál es la diferencia de electronegatividad para que un enlace se considere iónico?
- Copie los 4 ejemplos de enlace iónico mostrados en la figura 5.
- Escriba la definición de enlace covalente.
- ¿Cómo se representan las cargas parciales?
- Dos átomos pueden compartir uno, dos o tres pares de electrones. ¿Cómo se representan estos enlaces?
- Escriba la definición de enlace covalente no polar y, además, copie los ejemplos mostrados en la figura 6.
- ¿Qué es un enlace puro?
- Escriba la definición de enlace covalente polar y, además, copie los ejemplos mostrados en la figura 7.
- ¿Qué es un enlace covalente coordinado?
- Copie la figura 8.
- Escriba la definición de enlace metálico y, además, las propiedades que se pueden explicar con él.
